cho bột sắt vào dd chứa 0,2 mol H2SO4 loãng phản ứng hoàn toàn ng ta thu được 1,68 lít khí H2 tính khối lượng sắt phản ứng và để có sắt trên ng ta phải dùng bao nhiêu gam sắt (III) oxit tác dụng với khí H2 dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.n_{H_2SO_4}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,2}{1}>\dfrac{0,075}{1}\\ \Rightarrow H_2SO_4dư\\ b.n_{Fe}=n_{H_2}=0,075\left(mol\right)\\ m_{Fe}=56.0,075=4,2\left(g\right)\\ c.PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ 0,025........0,075.......0,05.......0,075\left(mol\right)\\ m_{Fe_2O_3}=0,025.160=4\left(g\right)\)

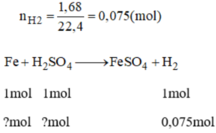
Theo phương trình phản ứng ta có:
n F e = n H 2 = 0,075 mol
n H 2 S O 4 = 0,075 mol (mà H 2 S O 4 đề cho là 0,2 mol nên H 2 S O 4 dư)
![]()

a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,075\left(mol\right)\Rightarrow m_{Fe}=0,075.56=4,2\left(g\right)\)
c, \(n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,075\left(mol\right)\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2-0,075=0,125\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,125.98=12,25\left(g\right)\)

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3
a)\(m_{Fe}=0,3\cdot56=16,8g\)
b)\(Fe_2O_3+3H_2\rightarrow3Fe+3H_2O\)
0,1 0,3 0,3
\(m_{Fe_2O_3}=0,1\cdot160=16g\)
a)nH2 =6,72:22,4=0,3(mol)
PTHH Fe+H2SO4--->FeSO4+H2
theo pt , nFe = nH2 = 0,3 (mol)
=> mFe =n.M=0,3.56=16,8(g)
b) Ta có nH2=nFe=0,3(MOL)
Pthh: Fe2O3 + 3H2 ---> 2Fe + 3H2O
theo pt , nFe2O3=1/3 nH2=0,1(mol)
=> mFe2O3= n.M=0,1.(56.2+16.3)=16(g)
Vậy để có lượng sắt tham gia phản ứng trên phải có 16g Fe2O3 để tác dụng với H2

a, Ta có pt pư
\(Fe+H_2SO_4-->FeSO_4+H_2\)
Ta có
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\)
=> \(H_2SO_4\) dư
\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{dư\left(H_2SO_4\right)}=19,6-14,7=4,9\left(g\right)\)
b,
Ta có
\(m_{Fe}=0,15\cdot56=8,4\left(g\right)\)

Fe+H2SO4-->FeSO4+H2
theo PTHH=> nH2SO4=nFE=0,2mol
=>mFe=0,2.56=11,2gam
c) Fe2O3 + 3H2---> 2Fe +3 H2O
nFe=0,2 mol.Theo PTHH=> nFe2O3=0,1mol
=> KL Fe2O3 cần dùng là 0,1.160=16gam
Ta có: nH2SO4=0,2 (mol) (theo đầu bài)
PT:
Fe + H2SO4 -> FeSO4 + H2
1...........1.............1............1 (mol)
0,2 <- 0,2 -> 0,2 -> 0,2 (mol)
b) mFe=n.M=0,2.56=11,2(gam)
c) PT:
Fe2O3 + 3H2 -t0-> 2Fe + 3H2O
1................3..............2..............3 (mol)
0,1 <- 0,3 <- 0,2 -> 0,3 (mol)
=> mFe2O3=n.M=0,1.160=16(g)
Vậy khối lượng Fe2O3 cần dùng là 16 gam
Phải dùng 4,2 g Fe
Cần 6g sắt (III) oxit tác dụng với H2 dư