giúp em 2 bài luôn nhé !
1) ngâm 1 vạt bằng đồng có khối lượng 5 gam tong 5oo gâm dung dịch AgNO3 4%. chỉ sau 1 lúc người ta lấy vật ra và thấy khối lượng AgNO3 trong dung dịch giảm mất 85%
a) tính khối lượng vật lấy ra sau khi làm khô
b) tính nồng đọ phần trăm các chất trong dung dịch sau khi lấy vật ra khỏi dung dịch
2) khi khử 15,2 gam hỗn hợp Fe2O3 và FeO bằng hidro ở nhiệt độ cao thu được sắt kim loại. để hòa tan hết lượng sắt này cần dùng 200ml dung dịch HCl nồng độ 2M
a) xác định thành phần phần trăm khối lượng mỗi oxit trong hỗn hợp
b) tính thể tích khí H2 (đktc) cần dùng để khử hỗn hợp trên

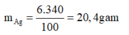
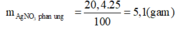
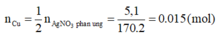
bài 1 (mk chưa học nên chép trên mạng)
Cu + 2AgNO3 => Cu(NO3)2 + 2Ag
mAgNO3= 20g
=>mAgNO3 giảm đi cũng là mAgNO3 PƯ'= 20 * 85% = 17g
=>nAgNO3= 0,1 mol
=>nCu = 0,05 => mCu = 3,2
nAg = 0,1
=> mAg = 10,8
=> khối lượng vật là 5 + 10,8 - 3,2 = 12,6 g
b) trong dung dịch có AgNO3 dư và Cu(NO3)2
mdd= 500 - 10,8 + 3,2 = 507,6 g
Bạn tự tính tiếp nhé