cho 68 g hỗn hợp 2 muối Cuso4 và mgso4 tác dụng với 1 lít dd chứa KOH 1 M và Naoh 0,4 M. sau phản ứng thu được 37 g kết tủa và dung dịch B. tính thành phần phần trăm khối lương cuso4 và mgso4 trong hỗn hợp đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi \(\left\{{}\begin{matrix}n_{NaOH}=a\left(mol\right)\\n_{KOH}=b\left(mol\right)\end{matrix}\right.\)
\(n_{Mg\left(OH\right)_2}=\dfrac{14,5}{58}=0,25\left(mol\right)\)
PTHH:
2NaOH + MgSO4 ---> Mg(OH)2 + Na2SO4
a -----------------------------> 0,5a
2KOH + MgSO4 ---> Mg(OH)2 + K2SO4
b -------------------------------> 0,5b
Hệ pt \(\left\{{}\begin{matrix}40a+56b=24,8\\0,5a+0,5b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{NaOH}=0,2.40=8\left(g\right)\\m_{KOH}=0,3.56=16,8\left(g\right)\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\%m_{NaOH}=\dfrac{8}{24,8}=32,26\%\\\%m_{KOH}=100\%-32,26\%=67,74\%\end{matrix}\right.\)
2NaOH+MgSO4->Mg(OH)2+Na2SO4
x-----------------------------1\2x
2KOH+MgSO4->K2SO4+Mg(OH)2
y--------------------------------------1\2y
=> ta có :
\(\left\{{}\begin{matrix}40x+56y=24,8\\0,5x+0,5y=0,25\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
%mNaOH=\(\dfrac{0,2.40}{24,8}100\)=32,25%
=>%m KOH=67,75%

Câu 3 :
\(m_{ct}=\dfrac{10.80}{100}=8\left(g\right)\)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
a) Hiện tượng : Xuất hiện kết tủa trắng
Pt : \(2NaOH+MgSO_4\rightarrow Na_2SO_4+Mg\left(OH\right)_2|\)
2 1 1 1
0,2 0,1 0,1 0,1
\(n_{Mg\left(OH\right)2}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
⇒ \(m_{Mg\left(OH\right)2}=0,1.58=5,8\left(g\right)\)
b) \(n_{MgSO4}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
\(m_{MgSO4}=0,1.120=12\left(g\right)\)
\(m_{ddMgSO}=\dfrac{12.100}{10}=120\left(g\right)\)
c) \(n_{Na2SO4}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{Na2SO4}=0,1.142=14,2\left(g\right)\)
\(m_{ddspu}=80+120-5,8=194,2\left(g\right)\)
\(C_{Na2SO4}=\dfrac{14,2.100}{194,2}=7,31\)0/0
Chúc bạn học tốt
Câu 4 :
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2|\)
1 1 1 1
0,2 0,2
\(n_{H2SO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{H2SO4}=0,2.98=19,6\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{19,6.100}{20}=98\left(g\right)\)
\(V_{ddH2SO4}=\dfrac{98}{1,2}\simeq81,67\left(ml\right)\)
Chúc bạn học tốt

Đáp án C
Ta có ![]()
![]()
=> mcác kim loại = ![]()
Chuỗi phản ứng: ![]()
![]()
![]()
![]()
=> nO oxi hóa FeO thành Fe2O3 =1,57 - 1,37 = 0,2 mol
Phản ứng: ![]()
= 0,2.2 = 0,4 mol
![]()
![]()

Đáp án C
G gồm Gly-Na và Ala-Na
Phản ứng với HCl :
Gly-Na + 2HCl -> H-Gly-HCl + NaCl
Mol a
Ala-Na + 2HCl -> H-Ala-HCl + NaCl
Mol b
=> nHCl =2a + 2b = 0,72 mol
Và mmuối = (111,5 + 58,5)a + (125,5 + 58,5)b = 63,72g
=> a = b = 0,18 mol
=> m + 12,24 = mGly-Na + mAla-Na
=> m = 25,2g
nNaOH = 0,36 mol = a + b
Bảo toàn khối lượng : mNaOH – mH2O =12,24g => nH2O = 0,12 mol = nX + nY
=> nX = nY = 0,06 mol
Gọi số mắt xích trong X là n => 0,06n + 0,06 = nGly + nAla = 0,36 mol
=> n = 5
+) TH1 : X là (Gly)3(Ala)2 và Y là Ala (loại vì mX = 19,86g < 20)
+) TH2 : X là (Gly)2(Ala)3 và Y là Gly (thỏa mãn vì mX = 20,7g)
=> %mX = 82,14%




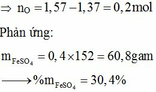
SO42- --->2OH-
96 2.17
M gỉam = 62
nSO4pu= (68-37)/62=0,5 mol
gọi CuSO4 là a mol, MgSO4 là b mol
có hệ a+b=0,5
160.a+120.b=68
suy ra a=0,2;b=0,3
%mCuSO4=0,2.160/68.100%47,06%
%mMgSO4=52,94%