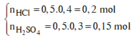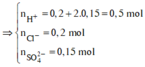Cho 100ml dd A chứa hỗn hợp HCl 0,1M và AlCl3 0,1M. Thêm V lít dd AgNO3 0,3M vào dd A thu được kết tủa lớn nhất là m gam. Tính giá trị nhỏ nhất của V và m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nNaHCO3=0,006 mol=nHCO3-
nK2CO3=0,012 mol=nCO32-
nH2SO4=0,3.0,02=0,006 mol=nSO42-
Tổng nH+ trong dd Y=0,02.0,4+0,02.0,3.2=0,02 mol
Cho từ từ dd axit vào dd muối 1 lúc sau mới có khí xuất hiện
H+ +CO32- =>HCO3-
Bđ:0,02 mol 0,012 mol
Pứ:0,012 mol<=0,012 mol=>0,012 mol
Dư: 0,008 mol
H+ +HCO3- =>CO2 + H2O
0,008 mol 0,018 mol
0,008 mol =>0,008 mol=>0,008 mol
0,01 mol
V=0,008.22,4=0,1792 lit=179,2ml
nKOH =nOH-=0,015 mol
nBaCl2 =0,25.0,15=0,0375 mol=nBa2+
OH- + HCO3- => CO32- +H2O
0,015 mol. 0,01 mol
0,01 mol<=0,01 mol=>0,01 mol
0,005 mol
Ba2+ + CO32- =>BaCO3
0,0375 mol 0,01 mol
0,01 mol<=0,01 mol=>0,01 mol
0,0275 mol
Ba2+ + SO42- =>BaSO4
0,0275 mol 0,006 mol
0,006 mol =>0,006 mol
mBaSO4=1,398g
mBaCO3=0,01.197=1,97g
Tổng m=3,368g
ChọnB

Đáp án B
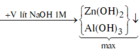
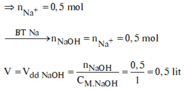
Ta có: nNaOH = 0,15 mol; nBa(OH)2 = 0,05 mol
Dung dịch Y chứa 0,15 mol Na+, 0,05 mol Ba2+, u mol AlO2- và v mol OH- dư
Định luật bảo toàn điện tích ta có u + v = 0,15 + 0,05.2 = 0,25 (1)
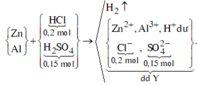
Ta có: nHCl = 0,32 mol và nH2SO4 = 0,04 mol→ nH+ = 0,4 mol; nSO4(2-) = 0,04 mol
→ nBaSO4 = 0,04 mol
Ta có: mkết tủa = 21,02 gam → nAl(OH)3 = 0,15 mol
Nếu Al(OH)3 chưa bị hòa tan thì nH+ = 0,4 = v + 0,15 (2)
Nếu Al(OH)3 đã bị hòa tan thì nH+ = 0,4 = v + 4u - 3.0,15 (3)
Giải hệ (1) và (2) ra vô nghiệm
Giải hệ (1) và (3) ra u = 0,2 và v = 0,05
Vậy Y gồm Na+ 0,15 mol; 0,05 mol Ba2+; 0,2 mol AlO2- và OH- dư (0,05 mol)
V lít dung dịch Z gồm 0,64V mol HCl và 0,08V mol H2SO4
→ nH+ = 0,8V mol và nSO4(2-) = 0,08 V mol
Khi Al(OH)3 max thì 0,8V = u+ v suy ra V = 0,3125
Suy ra nBaSO4 = 0,025 mol → mkết tủa = 21,425 gam
Khi BaSO4 max thì 0,08V = 0,05 suy ra V = 0,625
Suy ra nH+ = 0,8V = v + 4u-3.nAl(OH)3 → nAl(OH)3 = 7/60 mol → mkết tủa = 20,75 gam
Vậy mkết tủa max = 21,425 gam

Đáp án là A
nAl3+ = 0.04mol n(So4)2- = 0.06 mol n Oh - ban dau Ba chua Pu = 0.12 mol
vi De ket tua sinh ra lon nhat thi n Baso4 = 0.06 mol khi do nOh - =0.24 mol
noh- lớn hơn 4n Al 3+ => kết tủa Aloh)3 tan hết
m kettua = m BaSo4 max = 0.06*233= 13.98 g => m Ba = 0.06*137=8.22 g

nBa(OH)2=0,03 mol, nKOH=0,03 mol, nNaOH=x (mol)
=> Tổng số mol OH-=2*nBa(OH)2+nKOH+nNaOH=0,03*2+0,03+x=0,09+x (mol)
Để kết tủa lớn nhất => Tất cả Al3+ tạo Al(OH)3
Al3+ + 3OH- -> Al(OH)3↓
a------>3a--------->a (mol)
=> Tổng số mol OH-=3a=>0,09+x=a mol =>x=....
Đề này em cho thiếu nồng độ muối nhôm, xem lại đề và tìm số mol Al3+ thay vào chỗ a mà giải tiếp nha e

Giải thích:
Dd X + NaOH → Mg(OH)2 + Al(OH)3
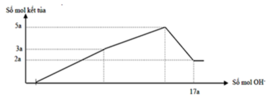
Lượng kết tủa khi NaOH dư là nMg(OH)2 = 2a
→ lượng kết tủa tối đa là nAl(OH)3 = n↓ - nMg(OH)2 = 5a - 2a =3a
→ nMg : nAl2O3 = 2a : = 4 : 3
Mà mhỗn hợp = 24nMg + 102nAl2O3 = 12,06 → nMg = 0,12 mol và nAl2O3 = 0,09 mol
→ a = 0,06 mol → nOH = 17a = 1,02 = nH+ (X) + 2nMg + 8nAl2O3 = nH+(X) + 0,96 → nH+(X) = 0,06 mol
Bảo toàn điện tích trong dung dịch X có nH+(X) + 2nMg2+ + 3nAl3+ = nCl- + 2nSO4 = 0,84
Mà nCl : nSO4 = 5 : 1 nên nCl- = 0,6 mol và nSO4 = 0,12 mol
X có Cl- : 0,6 mol SO42- : 0,12 mol, H+ : 0,06 mol, Al3+ : 0,18 mol và Mg2+ : 012 mol
Dd thêm vào có Ba2+ : x mol, Na+ : 3x mol ; OH- : 5x mol
Để thu được kết tủa tối đa thì ta có tạo kết tủa Al(OH)3 và Mg(OH)2 tối đa
nOH- = 5x = 0,18.3 +0,12.2 =0,78 mol
Khi đó Ba2+ : 0,156 → nBaSO4= 0,12 → ↓ BaSO4 : 0,12 mol; Al(OH)3 : 0,18 mol; Mg(OH)2 : 0,12 mol
→ nung thu được 0,12 mol BaSO4; 0,09 mol Al2O3 và 0,12 mol MgO
→ m =41,94
Đáp án D