TD 5: cho 4 lít N2 và 14 lít H2 vào bình kín rồi nung nóng với xúc tác thích hợp để phản ứng xảy ra , sau phản ứng thu được 16,4 lít hỗn hợp khí ( các khí đo ở cùng đều kiện về nhiệt độ và áp suất)
a. Tính thể tích khí amoniac thu được
b. Xác định hiệu suất của phản ứng.

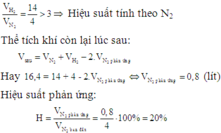
a) PTHH: N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Đặt thể tích N2 phản ứng là x (lít)
=> VH2 pứ= 3x (lít) , VNH3 sinh ra=2x (lít)
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được sau phản ứng là:
V khí= VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4
=> x=0,8 lít
=>VNH3 sinh ra= 2x = 2.0,8 =1,6 (lít)
b)Do \(\dfrac{4}{1}< \dfrac{14}{3}\) =>Hiệu suất tính theo N2
=>H=\(\dfrac{V_{N_2\left(pứ\right)}}{V_{N_2\left(bđ\right)}}\)⋅100=\(\dfrac{0,8}{4}.100\)=20%