Để thu được muối photphat trung hòa, cần lấy bao nhiêu ml dung dịch NaOH 1M cho tác dụng với 50ml dung dịch H3PO4 0,5M?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tham khảo
để thu được muối photphat trung hòa , cần lấy bao nhiêu ml dung dịch NaOH 1M cho tác dụng với 50ml dung dịch H3PO4 0,5M ? - Hoc24

Ta có: nH3PO4 = 0,05.0,5 = 0,025(mol)
Phương trình phản ứng:
H3PO4 + 3NaOH → Na3PO4 + 3H2O
Từ ptpư suy ra:
nNaOH = 3nH3PO4 = 3. 0,025 = 0,075 (mol)
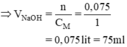

Số mol H3PO4: 0,050 x 0,50 = 0,025 (mol).
H3PO4 + 3NaOH → Na3PO4 + 3H2O
1 mol 3 mol
0,025 mol 3 x 0,025 mol
Thể tích dung dịch NaOH: 0,075 lít hay 75 ml

nNaOH/nH3PO4 = 0,05/0,025 = 2 → Tạo muối Na2HPO4
→ mNa2HPO4 = 0,025.142 = 3,55g
Đáp án A

Đáp án B
n NaOH= 0,2 mol
n H3PO4= 0,1 mol
n NaOH : nH3PO4= 2 : 1 nên chỉ xảy tạo muối Na2HPO4
=> n Na2PO4 = 0,1 mol => m =14,2

$n_{H_3PO_4} = 0,05.0,5 = 0,025(mol)$
$3NaOH + H_3PO_4 \to Na_3PO_4 + 3H_2O$
Theo PTHH :
$n_{NaOH} = 3n_{H_3PO_4} = 0,075(mol)$
$V_{dd\ NaOH} = \dfrac{0,075}{1} = 0,075(lít) = 75(ml)$