Đốt cháy hoàn toàn 7,8 gam este X thu được 11,44 gam CO2 và 4,68 gam H2O. Công thức phân tử của este là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
nCO2 = 0,26 mol ; nH2O = 0,26 mol
Bảo toàn nguyên tố : nC = 0,26 ; nH = 0,52 mol
Có : mX = mC + mH + mO => nO = 0,26 mol
=> nC : nH : nO = 0,26 : 0,52 : 0,26 = 1 : 2 : 1
=> Este có dạng : CnH2nOn và (pi + vòng) = 1 => este đơn chức
=> C2H4O2 thỏa mãn : HCOOCH3
Đáp án A

Đáp án: C
n
C
O
2
=
n
H
2
O
=
0
,
26
Như vậy, este là no, đơn chức
Gọi công thức este là CnH2nO2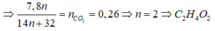

Đáp án : C
Este no, đơn chức, mạch hở: CnH2nO2
CnH2nO2 + [(3n - 2)/2 ]O2 → n CO2 + n H2O
0,26/n 0,26
=> (0,26/ n)(14n + 32) = 7,8
<=> n = 2
Este là C2H4O2

Đề đúng phải cho mCO2 = 11,44 (g)
Ta có : \(n_{CO_2}=n_{H_2O}=0,26\left(mol\right)\)
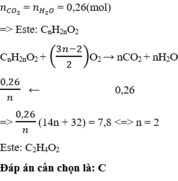
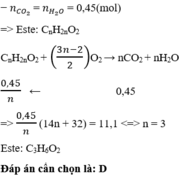
=> Este X là no, đơn chức. Gọi CTPT của Este là \(C_nH_{2n}O_2\)
\(\Rightarrow\frac{7,8n}{14n+32}=n_{CO_2}\Rightarrow\frac{7,8n}{14n+32}=0,26\Rightarrow n=2\)
Vậy công thức phân tử của Este X là \(C_2H_4O_2\)
=> Chọn C


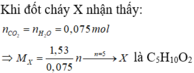
n co2 = nC = 0.26 mol
nh =2 n h2o = 2*0.26 = 0.52mol
m O = 7.8 - 0.26*12- 0.52*1 = 4.16 g
n O = 0.26 mol n C/ n H / n O = 1/2/1 => CTdon gian la ( CH2O)n vi X la este nen n> 1 ma este thi so O phai bang 2 nen chon n= 2 => CTPT c
2h4o2