Hỗn hợp A có N2 và 2 hidrocacbon nối tiếp , có khối lượng mA=13.8g và VA LÀ 11.2L. Trộn A với O2 dư rồi đốt , đc 11.7g H2O và 21.28l CO2
Xđ CTPT ,tình % khối lượng của từng hidrocacbon trong A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\( n_{H_2O} = \dfrac{11,7}{18} = 0,65\ mol\\ n_{CO_2} = \dfrac{17,6}{44} = 0,4\ mol\\ \Rightarrow Hidrocacbon :\ C_nH_{2n+2}\\ n_{hidrocacbon} = n_{H_2O} - n_{CO_2} = 0,65 - 0,4 = 0,25(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_{hidrocacbon}} = \dfrac{0,4}{0,25} = 1,6\\ 1< n=1,6<2\Rightarrow Hidrocacbon:\ CH_4,C_2H_6\\ n_{CH_4} = a\ mol ; n_{C_2H_6} = b(mol)\\ \Rightarrow a + b = 0,25 ; n_{CO_2} =a + 2b = 0,4\\ \Rightarrow a = 0,1 ; b = 0,15\\ \Rightarrow \%m_{CH_4} = \dfrac{0,1.16}{0,1.16+0,15.30}.100\% = 26,23\%\)
\(\%m_{C_2H_6} = 100\% - 26,23\% = 73,77\%\)

\(n_{CO_2}=\dfrac{48,4}{44}=1,1\left(mol\right)\\ n_{H_2O}=\dfrac{29,7}{18}=1,65\left(mol\right)\\ Vì:n_{H_2O}>n_{CO_2}\Rightarrow hhZ:hh.ankan\\ CTTQ:C_aH_{2a+2}\\ Ta.có:1< \dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1,65}{1,1}=1,5< 2\\ \Rightarrow hh.Z:50\%V_{CH_4},50\%V_{C_2H_6}\\ \Rightarrow\%m_{\dfrac{CH_4}{hhZ}}=\dfrac{16}{16+28}.100\approx36,364\%\\ \Rightarrow\%m_{\dfrac{C_2H_6}{hhZ}}\approx63,636\%\)

Với bài toán cho tỉ lệ thể tích, số mol như vậy thì đầu tiên ta sẽ dùng phương pháp tự chọn lượng chất để giải cho đơn giản:
+ Chọn nA =1,5 mol; nB = 3,2 mol
-------------\\\\\\\\\\\O2 : 32 48 – 38 =10
= 9,5.4 = 38
O3 : 48 38 – 32 = 6

Ta có: 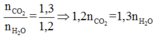
+ Thấy ngay dấu hiệu bảo toàn nguyên tố O:
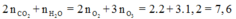
Ta có hệ phuơng trình sau:
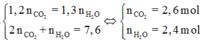
+ Bảo toàn khối luợng kết hợp bảo toàn nguyên tố C, H ta có:
![]()
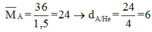
Đáp án A

Đáp án A
nO2=0,3125 mol
BTKL=>mN2=3,17+0,3125.32-12,89=0,28 gam=>nN2=0,01 mol=>n amin=0,02 mol => n hiđrocacbon=0,1 mol
- Giả sử số mol CO2 và H2O lần lượt là x, y
44x+18y=12,89
0,3125.2=2x+y (BTNT: O)
=>x=0,205; y=0,215
Ctb=0,205/0,12=1,7 => CH4
Htb=0,215/0,12=1,8 => C2H2 (Do số liên kết pi nhỏ hơn 3)
Đặt:
C2H7N: a
C3H9N: 0,02-a
CH4: b
C2H2: 0,1-b
+ BTNT C: 2a+3(0,02-a)+b+2(0,1-b)=0,205
+ BTNT H: 7a+9(0,02-a)+4b+2(0,1-b)=0,215.2
=>a=0,015;b=0,04 => CH4 (0,04 mol) C2H2 (0,06 mol)
=>%mC2H2=0,06.26/(0,06.26+0,04.16)=71%

Số mol
C
O
2
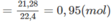
Khối lượng C trong A là: 0,95.12 = 11,4 (g).
Số mol
H
2
O
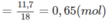
Khối lượng H trong A là: 0,65.2 = 1,3 (g).
Tổng khối lượng của C và H chính là tổng khối lượng 2 hiđrocacbon. Vậy, khối lượng N2 trong hỗn hợp A là : 18,30 - (11,4 + 1,3) = 5,6 (g)
Số mol
N
2
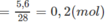
Số mol 2 hidrocacbon 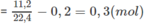
Đặt lượng C x H y là a mol, lượng C x + 1 H y + 2 là b mol :
a + b = 0,2 (1)
Số mol C = số mol C O 2 , do đó :
xa + (x + 1)b = 0,95 (2)
Số mol H = 2.số mol H 2 O , do đó :
ya + (y + 2)b = 2. 0,65= 1,3
Từ (2) ta có x(a + b) + b = 0,95 ⇒ b = 0,95 - 0,3x
Vì 0 < b < 0,3, nên 0 < 0,95 - 0,3x < 0,3
Từ đó tìm được 2,16 < x < 3,16 ⇒ x = 3.
⇒ b = 0,95 − 3.0,3 = 5. 10 - 2
⇒ a = 0,3 − 0,05 = 0,25
Thay giá trị tìm được của a và b vào (3), ta có y = 4.
% về khối lượng của C 3 H 4 trong hỗn hợp A:

% về khối lượng của C 4 H 6 trong hỗn hợp A :


\(Coi\ n_B = 1(mol) \\ n_{CO_2} = 1.30\% =0,3(mol) ; n_{H_2O} = 1.20\% = 0,2(mol)\\ A: C_nH_{2n+2-2k}\\\ n_C = n_{CO_2} = 0,3(mol)\\ n_H = 2n_{H_2O} = 0,4(mol)\\ Ta có : \dfrac{n}{2n+2-2k} = \dfrac{0,3}{0,4}\\ \Leftrightarrow 0,4n = 0,6n + 0,6 - 0.6k\\ \Leftrightarrow 0,6k -0,2n = 0,6\\ \Leftrightarrow 6k - 2n = 6\)
Với k = 1 thì n = 0(loại)
Với k = 2 thì n = 3(chọn)
Với k = 3 thì n = 6(chọn)
.....
Vậy hidrocacbon có thể là : \(C_3H_4 ; C_6H_8,...\)
\(Coi\ n_B = 1(mol)\\ \Rightarrow n_{CO_2} = 1.30\% = 0,3(mol) ; n_{H_2O} = 20\% = 0,2(mol) ; n_{O_2} = 50% = 0,5(mol)\)
Vì \(n_{CO_2} > n_{H_2O} \Rightarrow A: C_nH_{2n-2}\)
\(n_A = n_{CO_2} - n_{H_2O} = 0,3 - 0,2 = 0,1(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_A} = \dfrac{0,2}{0,1} = 2\\ CTPT\ A: C_2H_2\)

Đáp án A
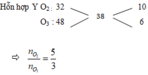
Giả sử số mol của Y = 0,8 mol => nX = 0,4mol
Bảo toàn nguyên tố O => 2nO2 + 3nO3 = 2nCO2 + nH2O = 1,9
nCO2 : nH2O = 6:7
=> nCO2 = 0,6 và nH2O = 0,7 mol
mX = mC + mH = 0,6 . 12 + 0,7 . 2 = 8,6g
=> MX = 8,6 : 0,4 = 21,5
dX/H2 = 10,75