Dẫn 13.44l A gồm H2 , 1 ankan và 1 anken qua Ni,to đc 10.08l hh khí B . Dẫn B qua bình nước brom thì màu của dd nhạt đi,khối lượng của bình tăng thêm 3.15g , còn lại 8.4l hh khí C ,dC/H2=17.8.(pư xảy ra hoàn toàn) Xđ CTPT và %Vtừng chất trong hh A ,B,C
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol khí trong hỗn hợp A là 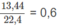
trong B là 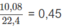
và trong C là 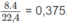
A chứa H 2 , C n H 2 n + 2 và C m H 2 m . Khi A đi qua chất xúc tác
Ni:
C m H 2 m + H 2 → C m H 2 m + 2
B chứa C n H 2 n + 2 , C m H 2 m + 2 và C m H 2 ra còn dư.
Số mol H 2 trong A là: 0,6 - 0,45 = 0,15 (mol).
Đó cũng là số mol C m H 2 m + 2 trong B.
Khi B đi qua nước brom thì C m H 2 m bị giữ lại:
C m H 2 m + B r 2 → C m H 2 m B r 2 .
Số mol C m H 2 m trong B là: 0,45 - 0,375 = 0,075 (mol).
Khối lương 1 mol
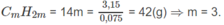
Anken là C 3 H 6 và ankan do chất đó tạo ra là C3H8.
Trong hỗn hợp c có 0,15 mol C 3 H 8 và 0,375 - 0,15 = 0,225 mol C n H 2 n + 2
Khối lượng hỗn hợp C là: 0,375. 17,8. 2 = 13,35 (g).
⇒ 0,15.44 + 0,225(14n + 2) = 13,35
⇒ n = 2 Ankan là C 2 H 6 .
A chứa C 2 H 6 (37,5%); C 3 H 6 (37,5%) và H2 (25%) ;
B chứa C 2 H 6 (50%); C 3 H 8 (33,3%) và C 3 H 6 (16,7%); C chứa C 2 H 6 (60%) và C 3 H 8 (40%).

1.GS có 100g dd $HCl$
=>m$HCl$=100.20%=20g
=>n$HCl$=20/36,5=40/73 mol
=>n$H2$=20/73 mol
Gọi n$Fe$(X)=a mol n$Mg$(X)=b mol
=>n$HCl$=2a+2b=40/73
mdd sau pứ=56a+24b+100-40/73=56a+24b+99,452gam
m$MgCl2$=95b gam
C% dd $MgCl2$=11,79%=>95b=11,79%(56a+24b+99,452)
=>92,17b-6,6024a=11,725
=>a=0,13695 mol và b=0,137 mol
=>C%dd $FeCl2$=127.0,13695/mdd.100%=15,753%
2.Bảo toàn klg=>mhh khí bđ=m$C2H2$+m$H2$
=0,045.26+0,1.2=1,37 gam
mC=mA-mbình tăng=1,37-0,41=0,96 gam
HH khí C gồm $H2$ dư và $C2H6$ không bị hấp thụ bởi dd $Br2$ gọi số mol lần lượt là a và b mol
Mhh khí=8.2=16 g/mol
mhh khí=0,96=2a+30b
nhh khí=0,06=a+b
=>a=b=0,03 mol
Vậy n$H2$=n$C2H6$=0,03 mol

Số mol các chất trong A là: 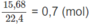
Khi A qua chất xúc tác Ni :
Hỗn hợp B chứa 3 chất: ankan ban đầu
C
n
H
2
n
+
2
, ankan mới tạo ra
C
m
H
2
m
+
2
và anken còn dư
C
m
H
2
m
với số mol tổng cộng là : 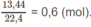
Số mol H 2 trong A là: 0,7 - 0,6 = 0,1(mol).
Khi B qua nước brom thì anken bị giữ lại hết:
C m H 2 m + B r 2 → C m H 2 m B r 2
Hỗn hợp C chỉ còn
C
n
H
2
n
+
2
và
C
m
H
2
m
+
2
với tổng số moi là 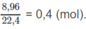
Như vậy, 0,2 mol C m H 2 m có khối lượng 5,6 g, do đó 1 mol C m H 2 m có khối lượng 28 (g) ⇒ m = 2.

a) \(m_{tăng}=m_{C_2H_4}=0,84\left(g\right)\)
=> \(n_{C_2H_4}=\dfrac{0,84}{28}=0,03\left(mol\right)\)
Gọi số mol CH4, H2 trong 3360 ml A là a, b
=> \(a+b=\dfrac{3,36}{22,4}-0,03=0,12\left(mol\right)\) (1)
Gọi số mol CH4, H2 trong 0,7 lít hh là ak, bk
=> ak + bk + 0,03k = \(\dfrac{0,7}{22,4}=0,03125\) (2)
Và 16ak + 2bk + 0,84k = 0,4875 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,09\left(mol\right)\\b=0,03\left(mol\right)\\k=\dfrac{5}{24}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,03}{0,15}.100\%=20\%\\\%V_{CH_4}=\dfrac{0,09}{0,15}.100\%=60\%\\\%V_{H_2}=\dfrac{0,03}{0,15}.100\%=20\%\end{matrix}\right.\)
b)
\(n_{C_2H_4}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
\(n_{CH_4}=\dfrac{1,68}{22,4}.60\%=0,045\left(mol\right)\)
\(n_{H_2}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
Bảo toàn C: \(n_{CO_2}=0,075\left(mol\right)\)
Bảo toàn H: \(n_{H_2O}=0,135\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,05.1=0,05\left(mol\right)\)
\(m_{ddCa\left(OH\right)_2}=1000.1,025=1025\left(g\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,05---->0,05----->0,05
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,025<--0,025------------>0,025
\(m_{CaCO_3}=\left(0,05-0,025\right).100=2,5\left(g\right)\)
mdd sau pư = 1025 + 0,075.44 + 0,135.18 - 2,5 = 1028,23 (g)
\(C\%_{Ca\left(HCO_3\right)_2}=\dfrac{0,025.162}{1028,23}.100\%=0,3939\%\)

1. Giả sử trong 20,16 lít A có x mol C 2 H 2 và y mol H 2 .
Ta có: 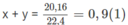
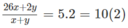
Giải hệ phương trình ta có x = 0,3 ; y = 0,6.
Thành phần hỗn hợp A:
C
2
H
2
chiếm 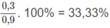
H 2 chiếm 100% - 33,33% = 66,67%
Khi A qua chất xúc tác Ni, xảy ra phản ứng cộng. C 2 H 2 hợp hiđro có thể tạo thành C 2 H 4 hoặc thành C 2 H 6 hoặc thành cả 2 chất đó :
C 2 H 2 + H 2 → C 2 H 4
C 2 H 2 + 2 H 2 → C 2 H 6
Số mol khí trong hỗn hợp B : 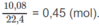
Trong hỗn hợp A có 0,3 mol C 2 H 2 thì trong hỗn hợp B cũng có 0,3 mol các hiđrocacbon.
Số mol H 2 trong B là: 0,45 - 0,3 = 0,15 (mol).
Số mol H 2 đã tham gia phản ứng: 0,6 - 0,15 = 0,45 (mol).
Khi B đi qua nước brom dư, những hiđrocacbon không no đều bị giữ lại hết (phản ứng hoàn toàn).
Vậy hỗn hợp C chỉ còn lại C 2 H 6 và H 2 với số mol tổng cộng là:

trong đó số mol H 2 là 0,15 mol, vậy số mol C 2 H 6 là : 0,33 - 0,15 = 0,18 (mol).
Thành phần hỗn hợp C:
C2H6 chiếm 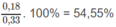
H2 chiếm 100% - 55,45% = 45,45%.
Trong hỗn hợp B cũng phải có 0,18 mol C 2 H 6 . Để tạo ra 0,18 mol C 2 H 6 cần 0,36 mol H 2 tác dụng với C 2 H 2 . Vậy lượng H 2 tác dụng với C 2 H 2 để tạo ra C 2 H 4 là : 0,45 - 0,36 = 9. 10 - 2 (mol).
Lượng C 2 H 4 trong hỗn hợp B là 9. 10 - 2 (mol) và lượng C 2 H 2 trong B là :
0,3 - 0,18 - 9. 10 - 2 = 3. 10 - 2 mol.
Thành phần hỗn hợp B:
C
2
H
6
chiếm 
C
2
H
4
chiếm 
C
2
H
2
chiếm 
H
2
chiếm 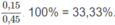
2. Khối lượng bình đựng nước brom tăng thêm :
9. 10 - 2 .28 + 3. 10 - 2 .26 = 3,3 (g).

- Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\Rightarrow27a+24b=10,2\left(1\right)\)
Khí thu được sau p/ứ là khí H2: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
2 3 (mol)
a 3/2 a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
1 1 (mol)
b b (mol)
Từ hai PTHH trên ta có: \(\dfrac{3}{2}a+b=0,5\left(2\right)\)
\(\left(1\right),\left(2\right)\) ta có hệ: \(\left\{{}\begin{matrix}27a+24b=10,2\\\dfrac{3}{2}a+b=0,5\end{matrix}\right.\)
Giải ra ta có \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
a) \(\%Al=\dfrac{m_{Al}}{m_{hh}}.100\%=\dfrac{0,2.27}{10,2}.100\%\approx52,94\%\)
\(\%Mg=100\%-\%Al=100\%-52,94=47,06\%\)
b)
\(3H_2+Fe_2O_3\rightarrow^{t^0}2Fe+3H_2O\)
3 1 2 (mol)
0,5 1/6 1/3 (mol)
\(m_{Fe}=\dfrac{1}{3}.56=\dfrac{56}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(pứ\right)}=\dfrac{1}{6}.160=\dfrac{80}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(dư\right)}=60-m_{Fe}=60-\dfrac{56}{3}=\dfrac{124}{3}\left(g\right)\)
\(a=\dfrac{124}{3}+\dfrac{80}{3}=68\left(g\right)\)

tỉ khối là 13 chứ
nX = 0,25
n↓ = nAnkin = 0,25.20% = 0,05
=>M↓ = 147: C3H3Ag
->Ankin là C3H4 (0,05 mol)
nY = 0,2; nCO2 = 0,3
=>Số C = nCO2/nY = 1,5
Ankan là CH4
mY = mX – mC3H4 = 4,5
=>nH2O = \(\dfrac{4,5}{0,3.12}.\dfrac{1}{2}\) = 0,45
nCH4 = nH2O – nCO2 = 0,15 và nCxH2x = nY – nCH4 = 0,05
nCO2 = 0,15.1 + 0,05x = 0,3
=>x = 3
=> Anken là C3H6

nX = 0.15
nZ = 0035
Xét đầu quá trình và cuối quá trình ko có chất nào bay lên hay kết tủa nên bảo toàn khối lượng ta có :
m X = m Y = m ( bình brom tăn lên ) + m Z
=> 0.15 * 10 * 2 = m ( bình brom tăng lên ) + 0.035 * 6.5 * 4
=> m ( bình brom tăng lên ) = 2,09 g
