Một bình có dung tích V=10 lít chứa một lượng khí hidro bị nén ở áp suất p=50at,7oC. Khi nung nóng bình, do bình hở nên có một phần khí thoát ra; phần khí còn lại có nhiệt độ 17oC và vẫn dưới áp suất như cũ. Tính khối lượng khí đã thoát ra.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi m1, m2 là khối lượng khí trong bình trước và sau khi nung nóng bình. Áp dụng phương trình Menđêlêep – Clapêrôn ta có:
p V = m 1 μ R T 1 , p V = m 2 μ R T 2 . ⇒ m 2 − m 1 = p V μ R ( 1 T 1 − 1 T 2 )
Với p = 50atm, V = 10 lít, μ = 2 g
R = 0 , 082 ( a t m . l / m o l . K ) Mà T 1 = 273 + 7 = 280 K ; T 2 = 273 + 17 = 290 K
⇒ m 2 − m 1 = 50.10.2 0 , 082 ( 1 280 − 1 290 ) m 2 - m 1 = 1 , 502 ( g )

Chọn D.
Gọi khối lượng khí trong bình trước và sau khi nung là m 1 , m 2 .
Áp dụng phương trình Cla-pê-rôn – Men-đê-lê-ép, ta có:


Gọi m i , rrn là khối lượng khí trong bình trước và sau khi nung nóng bình.
Áp dụng phương trình Menđêlêep - Clapêrôn ta có:
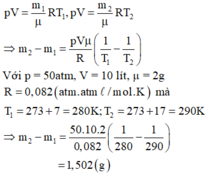

Chọn D.
Gọi khối lượng khí trong bình trước và sau khi nung là .
Áp dụng phương trình Cla-pê-rôn – Men-đê-lê-ép, ta có:

Suy ra độ biến thiên khối lượng khí trong bình là:
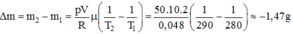
Dấu "–" cho biết khí thoát bớt ra khỏi bình.

Chọn đáp án C
? Lời giải:
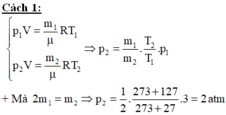
Cách 2:
Ta xét trạng thái của lượng khí còn lại trong bình sau khi nhiệt độ tăng lên 127 độ C. Khi đó nó chiếm thể tích cả bình.nhưng khi chưa mờ van và nhiệt độ trong bình còn 27 độ c thì nó chiếm một phần hai thể tích cả bình


Ta có
Trạng thái 1: { V 1 p 1 = 1 , 5 a t m T 1 = 27 + 273 = 300 K Trạng thái 2: { V 2 = V 1 2 p 2 = ? T 2 = 273 + 127 = 400 K
Áp dụng
p 1 V 1 T 1 p 2 V 2 T 2 ⇒ p 2 = p 1 V 1 T 2 T 1 V 2 = 1 , 5. V 1 .400 300.0 , 5. V 1 p 2 = 4 ( a t m )

+ Gọi v 0 là thể tích của bình
Ta xét trạng thái của lượng khí còn lại trong bình sau khi nhiệt độ tăng lên 127 độ C. Khi đó nó chiếm thể tích cả binh nhưng khi chưa mả van và nhiệt độ trong binh còn 27 độ C thì nó chiếm một phần hai thể tích cả bình.
Khi lượng khí đó ở nhiệt độ 27 ° C trạng thái 1


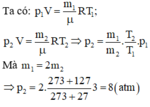
Gọi \(m_1;m_2\) là khối lượng khí trong bình trước và sau khi đun nóng bình. Áp dụng phương trình Menđêlêep - Clapêrông ta có: \(pV=\frac{m_1}{\mu}RT_1;pV=\frac{m_2}{\mu}RT_2\)
Từ đó suy ra khối lượng khí đã thoát ra:
\(m_2-m_1=\frac{pV\mu}{R}\left(\frac{1}{T_1}-\frac{1}{T_2}\right)\), với \(p=50atm,V=10\)lít \(,\mu=2g\)
\(R=0,084atm.l\text{/}mol.K;\)\(T_1=7+273=280K\)
\(T_2=17+273=290K\). Suy ra \(m_2-m_1=1,47g\)
Gọi m1,m2m1,m2 là khối lượng khí trong bình trước và sau khi đun nóng bình. Áp dụng phương trình Menđêlêep - Clapêrông ta có: pV=m1μRT1,pV=m2μRT2pV=m1μRT1,pV=m2μRT2
Từ đó suy ra khối lượng khí đã thoát ra:
m2−m1=pVμR(1T1−1T2)m2−m1=pVμR(1T1−1T2), với p=50atm,V=10lít,μ=2gp=50atm,V=10lít,μ=2g
R=0,084atm.l/mol.K;T1=7+273=280KR=0,084atm.l/mol.K;T1=7+273=280K
T2=17+273=290KT2=17+273=290K. Suy ra m2−m1=1,47g