Đốt cháy hoàn toàn 0,6g hợp chất hữu cơ X rồi cho sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy có 2 gam kết tủa và khối lượng bình tăng thêm 1,24 gam. Tỉ khooia của X so với H2 bằng 15. Công thức phân tử của X là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


còn thiếu nguyên tố Ôxi và bạn chưa hề sử dụng tới dữ kiện là có 0,6gam hợp chất hữu cơ X

Chọn đáp án D
nC = nCO2 = n↓ = 0,02 mol.
mbình tăng = mCO2 + mH2O
⇒ nH2O = (1,24 - 0,02 × 44) ÷ 18 = 0,02 mol
⇒ nH = 0,04 mol.
mX = mC + mH + mO ⇒ mO = 0,64(g)
⇒ nO = 0,02 mol.
⇒ C : H : O = 0,02 : 0,04 : 0,02 = 1 : 2 : 1
⇒ CT nguyên: (CH2O)n.
30n = 30 ⇒ n = 1 ⇒ CTPT của X là CH2O

$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CO_2} = n_{CaCO_3} = \dfrac{12}{100} = 0,12(mol)$
Ta có : $m_{bình\ tăng} = m_{CO_2} + m_{H_2O}$
$\Rightarrow m_{H_2O} = 8,16 - 0,12.44 = 2,88(gam)$
$\Rightarrow n_{H_2O} = 0,16(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow m_O = m_X - m_C - m_H = 1,28(gam) \Rightarrow n_O = \dfrac{1,28}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,12 : 0,32 : 0,08 = 3 : 8 : 2$
Vậy CTPT của X : $(C_3H_8O_2)_n$
$M_X = 76n = M_{H_2}.38 = 76 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_2$

a) X + O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
Từ pt => nCO2 = nCaCO3 = \(\dfrac{40}{100}\)= 0,4 mol => nC = 0,4 mol, mC= 0,4.12= 4,8gam.
Mà khối lượng bình tăng = mCO2 + mH2O ( vì cho CO2 và H2O vào bình).
=> mCO2 + mH2O = 26,6
<=> mH2O = 26,6 - 0,4.44= 9 gam , nH2O = \(\dfrac{9}{18}\)= 0,5 mol
=> nH = 2nH2O =1 mol => mH =1 gam
mC + mH = 5,8 = mX => X chỉ chứa cacbon và hidro
Gọi CTĐGN của X là CxHy <=> CTPT của X là (CxHy)n
x : y = nC : nH = 2 : 5=> CTPT X là (C2H5)n
Mà X có tỉ khối so với H2 = 29 => MX = 58
=> n =2 , CTPT của X là C4H10
b)
X có dạng CTPT CnH2n+2 => X là ankan
CTCT có thể của X
CH3-CH2-CH2-CH3 ; CH3-CH(CH3)-CH3

\(n_{CO_2}=n_{CaCO_3}=0,5\left(mol\right)\)
=> \(n_C=0,5\left(mol\right)\)
\(m_{binhtang}=m_{CO_2}+m_{H_2O}=0,5.44+m_{H_2O}=31\)
=> \(m_{H_2O}=9\left(g\right)\Rightarrow n_{H_2O}=0,5\left(mol\right)\)
=> \(n_H=1\left(mol\right)\)
\(M_A=16.6,375=102\)
\(m_O=10,2-0,5.12-0,5.2=3,2\left(g\right)\)
=>\(n_O=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz
Ta có : x:y:z = 0,5 :1 : 0,2 =2,5 : 5 :1 = 5 :10: 2
=> CTĐGN của A : (C5H10O2)n
Ta có : \(102.n=102\)
=> n=1
Vậy CTPT của A : C5H10O2

Quy đổi cứ 2 mol C2H4 thành 1 mol CH4 và 1 mol C3H4
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_3H_4}=b\left(mol\right)\end{matrix}\right.\)
=> 16a + 40b = 8,4
Và \(\overline{M}=\dfrac{8,4}{a+b}=14.2=28\left(g/mol\right)\)
=> a = 0,15 (mol); b = 0,15 (mol)
Bảo toàn C: nCO2 = 0,6 (mol)
=> m = 0,6.197 = 118,2 (g)
Bảo toàn H: nH2O = 0,6 (mol)
=> a = 0,6.44 + 0,6.18 = 37,2 (g)

a, \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)=n_C\)
⇒ mC + mH = 0,2.12 + 0,4.1 = 2,8 (g) < mA
→ A gồm C, H và O.
⇒ mO = 6 - 2,8 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,4:0,2 = 1:2:1
→ CTPT của A có dạng (CH2O)n
Không biết đề có cho thêm dữ kiện liên quan đến MA không bạn nhỉ?

Đáp án B
Vì sau phản ứng, dẫn sản phẩm cháy vào bình đựng PdCl2 thấy xuất hiện kết tủa nên trong sản phẩm thu được có chứa CO:
![]()
Tiếp tục dẫn khí qua bình 2 chứa dung dịch Ca(OH)2 dư xuất hiện kết tủa nên khí bị hấp thụ là CO2 gồm CO2 tạo thành từ phản ứng (1) và có thể gồm CO2 sản phẩm cháy:
![]()
![]()
![]()

![]()
![]()
![]()


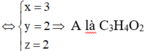


nCaCO3=0,02 mol=nCO2 ==>%C=(0,02.12):0,6=40%
m(bình tăng)=mCO2+mH2O=0,02.12+mH2O=1,24==>mH2O=0,36g
==>mH=(0,36.2):18=0,04 g
%H=6,67% =>%O=100-40-6,67=53,33%
CTĐGN CxHyOz
x:y:z=40/12 : 6,67 : 53,33/16
= 3,33 : 6,67 : 3,33 = 1: 2 : 1
=> CTĐGN : CH2O
CTPT : (CH2O)n M=30n=15.2 =>n=1
=> CTPT : CH2O