Bài 6: Hòa tan hoàn toàn m gam hỗn hợp X gồm 4 oxit bazơ cần dùng vừa đúng 1,6 lít dung dịch H2SO4 0,5M thu được dung dịch Y chứa 4 muối sunfat trung hòa. Cô cạn dung dịch Y được 107,4g muối khan. Xác định giá trị m?
Bài 7: Để trung hòa V ml dung dịch X gồm HCl 1M và H2SO4 0,5M thì cần 200 ml dung dịch Ba(OH)2 1M thu được m gam kết tủa, dung dịch Y. a) Tính V, m. b) Tính khối lượng muối khan thu được khi cô cạn dung dịch Y.
Bài 8: Cho 2,88 gam một kim loại X có hóa trị không đổi tác dụng với 300 ml dung dịch HCl 1M thu được dung dịch A. Để trung hòa vừa đủ trong dung dịch A cần 60 ml dung dịch NaOH 1M. Xác định tên kim loại X.


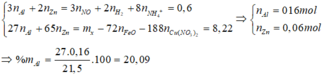
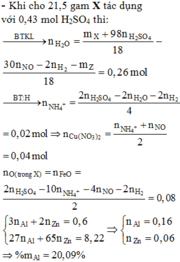
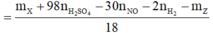



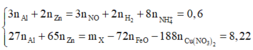

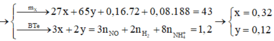



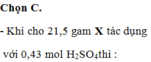
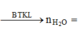
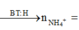
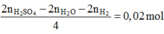
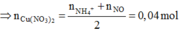
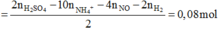

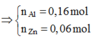
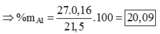

Bài 6 :
Bảo toàn nguyên tố H :
$n_{H_2O} = n_{H_2SO_4} =1,6.0,5 = 0,8(mol)$
Bảo toàn khối lượng :
$m = 107,4 + 0,8.18 - 0,8.98 = 43,4(gam)$
Bài 7 :
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$Ba(OH)_2 + H_2SO_4 \to BaSO_4 + 2H_2O$
$n_{HCl} = 0,001V(mol) ; n_{H_2SO_4} = 5.10^{-4}V(mol)$
Theo PTHH :
$n_{Ba(OH)_2} = \dfrac{0,001}{2} + 5.10^{-4}V = 10^{-3}V = 0,2$
$\Rightarrow V = 200(ml)$
$n_{BaSO_4} = n_{H_2SO_4} = 0,1(mol)$
$m = 0,1.233 = 23,3(gam)$
b)
$n_{BaCl_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$m_{BaCl_2} = 0,1.208 = 20,8(gam)$
Câu 8 :
$n_{HCl} = 0,3(mol)$
$HCl + NaOH \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,06(mol)$
$\Rightarrow n_{HCl\ pư} = 0,3 - 0,06 = 0,24(mol)$
Gọi n hóa trị của X
$2X + 2nHCl \to 2XCl_n + nH_2$
Theo PTHH :
$n_X = \dfrac{1}{n}.n_{HCl} = \dfrac{0,24}{n}(mol)$
$\Rightarrow \dfrac{0,24}{n}.X = 2,88 \Rightarrow X = 12n$
Với n = 2 thì $X = 24(Magie)$