Hòa tan hoàn toàn 3,78 gam một kim loại X bằng dung dịch HCl thu được 4,704 lít khí hidro( ở đktc). Xác định kim loại X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{H_2}=\dfrac{4,704}{22,4}=0,21\left(mol\right)\)
Giả sử KL X có hóa trị n.
PT: \(2X+2nHCl\rightarrow2XCl_n+nH_2\)
Theo PT: \(n_X=\dfrac{2}{n}n_{H_2}=\dfrac{0,42}{n}\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{3,78}{\dfrac{0,42}{n}}=9n\left(g/mol\right)\)
Với n = 3 thì MX = 27 (g/mol) là thỏa mãn.
Vậy: X là Al.

Gọi n là hóa trị của kim loại A và A cũng là phân tử khối của kim loại và a là số mol A đã dùng.
\(A+nHCl\rightarrow ACl_n+\frac{n}{2}H_2\)
\(1mol\) \(\frac{n}{2}mol\)
\(amol\) \(\frac{a.n}{2}mol\)
Ta có hệ:
\(\begin{cases}a.A=3,78\\\frac{a.n}{2}=\frac{4,704}{22,4}\end{cases}\)\(\Rightarrow\begin{cases}a.A=3,78\left(1\right)\\a.n=0,42\left(2\right)\end{cases}\)
Lấy \(\left(1\right)\) chia \(\left(2\right)\) ta có: \(\frac{A}{n}=9\Rightarrow A=9n\)
Vì hóa trị của kim loại chỉ có thể là 1 hoặc 2 hoặc 3. Do đó ta có bảng sau:
| n | 1 | 2 | 3 |
| A | 9(loại) | 18(loại) | 27(Nhận) |
Trong các kim loại trên chỉ có kim loại \(\left(Al\right)\) có hóa trị \(III\) ứng với nguyên tử khối là 27 là phù hợp. Vậy \(A\) là kim loại nhôm \(\left(Al\right)\)

Gọi hóa trị của kim loại A là x
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH : 2A + 2xHCl -----> 2AClx + xH2
0,2/x mol 0,1mol
Áp dụng m = n.M , ta có : \(A.\frac{0,2}{x}=6,5\Rightarrow A=32,5x\)
Do x là hóa trị của kim loại nên x chỉ có thể là I , II hoặc III
Nếu x = 1 thì A = 32,5 (loại)
Nếu x = 2 thì A = 65 (nhận)
Nếu x = 3 thì A = 97,5 (loại)
Vậy A là kim loại Kẽm (Zn)
chỗ áp dụng là sao v bạn..? mình kh hiểu..đang tính khối lượng à bạn?

Số mol của khí hidro ở dktc
nH2 =\(\dfrac{V_{H2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : X + 2HCl → XCl2 + H2\(|\)
1 2 1 1
0,1 0,1
Số mol của kim loại X
nX = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{n_X}=\dfrac{5,6}{0,1}=56\) (dvc)
Vậy kim loại x là Fe
⇒ Chọn câu : B Chúc bạn học tốt
\(R+2HCl \rightarrow RCl_2+H_2\\ n_{H_2}=\frac{2,24}{22,4}=0,1mol\\ M_R=\frac{5,6}{0,1}=56 g/mol\\ \Rightarrow R: Fe\)

2A+6HCl->2ACl3+3H2
0,2----0,6------------0,3 mol
n H2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>\(\dfrac{5,4}{A}\)=0,2
=>A=27 g\mol
=>A là nhôm (Al)
CMHCl=\(\dfrac{0,6}{0,5}\)=1,2M
\(5,4gA+500mlHCl->X:ACl3+6,72lH2\)
nH2 = 0,3 ( mol )
=> nAl = 2/3.nH2 = 0,2 ( mol )
( Cân bằng PTHH )
Ta có :
M = \(\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\)
=> Đó là Al

\(2X+2nHCl->2XCl_n+nH_2\\n_{H_2}=\dfrac{4,704}{22,4}=\dfrac{3,78}{X}\cdot\dfrac{n}{2}\\ n:X=\dfrac{1}{9}\\ n=3;X=27\\ X:Al\left(aluminium:nhôm\right) \)

a) Gọi công thức chung của 2 kim loại là R
PTHH: \(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(\Rightarrow n_R=0,1\left(mol\right)\) \(\Rightarrow\overline{M}_R=\dfrac{3,26}{0,1}=32,6\)
Ta thấy \(23< 32,6< 39\) \(\Rightarrow\) 2 kim loại cần tìm là Natri và Kali
b) PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
a_____________a______\(\dfrac{1}{2}\)a (mol)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\uparrow\)
b____________b______\(\dfrac{1}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}23a+39b=3,26\\\dfrac{1}{2}a+\dfrac{1}{2}b=0,05\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,06\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,04\cdot23}{3,26}\cdot100\%\approx28,22\%\\\%m_K=71,78\%\end{matrix}\right.\)
c) PT ion: \(OH^-+H^+\rightarrow H_2O\)
0,1____0,1
Ta có: \(n_{H^+}=n_{HCl}=0,1\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,1\cdot36,5}{5\%}=73\left(g\right)\)
 thì do nó bị kéo lại nên bạn sửa lại thế này này:
thì do nó bị kéo lại nên bạn sửa lại thế này này:
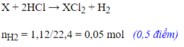
2X + 2nHCl ---> 2XCln + nH2
Nguyên tử khối X = 3,78n.22,4/2.4,704 = 9n
Vậy, n = 3. X = 27 (Al).
2X + 2nHCl ---> 2XCln + nH2
Nguyên tử khối X = 3,78n.22,4/2.4,704 = 9n
Vậy, n = 3. X = 27 (Al).