Hỗn hợp a dạng bột gồm Mg và Al lấy 12,6 gam A tác dụng vừa đủ với 300 ml dung dịch hỗn hợp HCL 1 mol trên lít và Al2 SO4 loãng c 2 mol trên lít biết C1 = 2 C2 sau phản ứng thu được dung dịch B và 13,44 l khí H2 điều kiện tiêu chuẩn a viết các phương trình hóa học xảy ra B xác định c1 c2 và phần trăm về khối lượng các chất trong hỗn hợp a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy đổi hỗn hợp B thành A l a : 0 , 1 m o l G l u : 0 , 15 m o l N a O H : 0 , 3 m o l
Tóm tắt: B A l a : 0 , 1 m o l G l u : 0 , 15 m o l N a O H : 0 , 3 m o l + H C l → M u ố i + H 2 O
n H C l = n A l a + n G l u + n N a O H = 0 , 1 + 0 , 15 + 0 , 3 = 0 , 55 m o l
n H 2 O = n N a O H = 0 , 3 m o l
B T K L → m m u o i = m B + m H C l −
→ m = 0,1.89 + 0,15.147 + 0,3.40 + 0,55.36,5 - 0,3.18 = 57,625 gam
Đáp án cần chọn là: D

Chọn đáp án B
Ta có:
nHCl pứ = nNaOH + nAlanin + nAxit glutamic
⇒ nHCl pứ = 0,3 + 0,1 + 0,15 = 0,55 mol.
+ nNaOH pứ = nH2O = 0,3 mol.
⇒ Áp dụng định luật BTKL ta có:
mChất rắn = mAlanin + mAxit glutamic + mNaOH + mHCl – mH2O.
mChất rắn = 0,1×89 + 0,15×147 + 0,3×40 + 0,55×36,5 – 0,3×18 = 57,625 gam
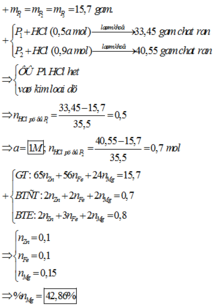

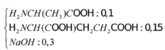
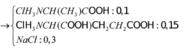


Ta có : C1=2C2
=> Gọi nH2SO4 =x
=> n HCl = 2x
Bảo toàn nguyên tố H :\(n_{HCl}.1+n_{H_2SO_4}.2=n_{H_2}.2\)
\(\Rightarrow2a+2a=\dfrac{13,44}{22,4}=0,6.2\)
=>a = 0,3(mol)
=> CMHCl = \(\dfrac{0,6}{0,3}=2M\); CMH2SO4 = \(\dfrac{0,3}{0,3}=1M\)
Dung dịch B gồm : Mg 2+ , Al3+ , Cl- , SO4 2-
\(n_{Cl^-}=n_{HCl}=0,6\left(mol\right);n_{SO_4^{2-}}=n_{H_2SO_4}=0,3\left(mol\right)\)
Bảo toàn điện tích cho dung dịch B:
\(n_{Mg}.2+n_{Al}.3=0,6+0,3.2\) (1)
Theo đề bài : \(24.n_{Mg}+27.n_{Al}=12,6\) (2)
Từ (1), (2)=> \(\left\{{}\begin{matrix}n_{Mg}=0,3\\n_{Al}=0,2\end{matrix}\right.\)
=> \(\%m_{Mg}=\dfrac{0,3.24}{12,6}.100=57,14\%\)
=> % m Al = 100 -57.14 = 42,86%