Dung dịch A chứa H2SO4 aM và HCl 0,2M ; dung dịch B chứa NaOH 0,5M và Ba(OH)2 0,25M. Biết trộn 100ml dung dịch A với 120ml dung dịch B thì thu được dung dịch có pH =7. Giá trị của a là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Dung dịch sau khi trộn có pH =7 ⇒ nOH- = nH+
⇒ 2a.0,1 + 0,2.0,1 = 0,5.0,12 + 0,25.2.0,12
⇒ a = 0,5
Đáp án B.

Đáp án D
Dung dịch C có pH =7 ⇒ nH+ = nOH- ⇒ 0,1.0,1.2 + 0,2.0,1 = 0,2V + 0,3V
⇒ V =0,08l = 80 ml
Đáp án D.

Đáp án : D
Trong A :
n H + = 2 n H 2 S O 4 + n H N O 3 + n H C l = 0,21 mol
Trong B :
n O H - = nNaOH + nKOH = 0,49V mol
Để C có pH = 2 (axit) => H+ dư
=> nH+(C) = 10-pH .(0,3 + V) = 0,21 – 0,49V
=> V = 0,414 lit

\(n_{H^+}=0,07mol=n_{OH^-}\)=>\(v=\dfrac{0,07}{0,2+0,1.2}=0,175l\)

nOH- = (0,2 + 0,1.2)V = 0,4V; nH+ = (0,25.2 + 0,75).0,04 = 0,05
Do trung hòa nên nOH- = nH+ → 0,4V = 0,05 → V = 0,125 lít
Đáp án B



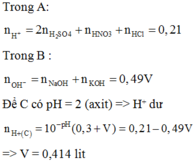
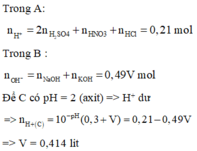
nH2SO4 = 0,1 . a (mol)
nHCl = 0,1 . 0,2 = 0,02 mol
nH+ = 2nH2SO4 + nHCl = 0,2a + 0,02 (mol)
nNaOH = 0,5 . 0,12 = 0,06 mol
nBa(OH)2 = 0,25 . 0,12 = 0,03 mol
nOH- = nNaOH + 2nBa(OH)2 = 0,12 mol
Trộn A với B:
H+ + OH- → H2O
Dung dịch sau phản ứng có pH = 7 nên H+ và OH- phản ứng vừa đủ với nhau
nH+ = nOH-
→ 0,2a + 0,02 = 0,12
→ a = 0,5