Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tỉ lệ về thể tích bằng tỉ lệ về số mol
Coi $n_{CO_2} = 4(mol) \Rightarrow n_{H_2O} = 3(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 4(mol) ; n_H = 2n_{H_2O} = 6(mol)$
$m_C = 4.12 = 48(gam)$
$\Rightarrow m_O = 48.\dfrac{2}{3} = 32(gam)$
$\Rightarrow n_O = \dfrac{32}{16} = 2(mol)$
Ta có :
$n_C : n_H : n_O = 4 : 6 : 2 = 2 : 3 : 1$
Vậy CTPT của A là $(C_2H_3O)_n$
Với n = 2 thì tồn tại CTCT : $OH-CH_2-C \equiv C-CH_2-OH$
Vậy CTPT là $C_2H_6O_2$

Ta có \(n_{CO_2}=\dfrac{8,8}{44}=0,2(mol);n_{H_2O}=\dfrac{3,6}{18}=0,2(mol)\)
Bảo toàn C và H: \(n_{C}=0,2(mol);n_{H}=0,4(mol)\)
\(\Rightarrow m_A=m_C+m_H=0,2.12+0,4.1=2,8<6\)
Do đó A chứa O
\(\Rightarrow m_O=6-2,8=3,2(g)\\ \Rightarrow n_O=\dfrac{3,2}{16}=0,2(mol)\)
Đặt \(CTHH_A:C_xH_yO_z\)
\(\Rightarrow x:y:z=0,2:0,4:0,2=1:2:1\\ \Rightarrow CTPT_A:CH_2O\)

Theo đề bài ta có 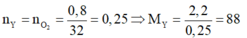
Vì sản phẩm cháy thu được CO2 và H2O nên Y chắc chắn chứa C, H, có thể có O.
Khối lượng các nguyên tố trong 4,4 gam chất Y là:
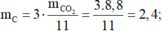
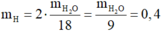
![]()
Gọi CTPT của chất Y là CxHyOz . ta có như sau:
Vậy ta có x = 4, y = 8 và z = 2
CTPT của Y là C4H8O2
Đáp án A.

a)
CTPT: CnH2n+2
\(\%C=\dfrac{12n}{14n+2}.100\%=83,72\%\)
=> n = 6
=> CTPT: C6H14
b)
\(n_{CH_4}=\dfrac{2,4}{16}=0,15\left(mol\right)\)
=> \(n_Y=0,15\left(mol\right)\)
=> \(M_Y=\dfrac{8,7}{0,15}=58\left(g/mol\right)\)
=> CTPT: C4H10
c) CTPT: CnH2n+2
Xét \(\dfrac{m_C}{m_H}=\dfrac{12.n}{1\left(2n+2\right)}=4\)
=> n = 2
=> CTPT: C2H6
d)
Giả sử các khí đo ở điều kiện sao cho 1 mol khí chiếm thể tích V lít
\(n_{C_nH_{2n+2}}=\dfrac{1}{V}\left(mol\right)\); \(n_{O_2}=\dfrac{6,5}{V}\left(mol\right)\)
PTHH: CnH2n+2 + \(\dfrac{3n+1}{2}\)O2 --to--> nCO2 + (n+1)H2O
=> \(\dfrac{1}{V}.\dfrac{3n+1}{2}=\dfrac{6,5}{V}\)
=> n = 4
=> CTPT: C4H10
e)
CTPT: CnH2n+2
=> CTPT của dẫn xuất monoclo: CnH2n+1Cl
=> \(\%Cl=\dfrac{35,5}{14n+36,5}.100\%=55,039\%\)
=> n = 2
=> CTPT: C2H6

\(Đặt:CTHH:C_xH_yO_z\)
\(x:y:z=\dfrac{52.17}{12}:\dfrac{13.04}{1}:\dfrac{34.78}{16}=4.3475:13.04:2.17375=2:6:1\)
\(CTđơngiản:\left(C_2H_6O\right)_n\)
\(M_Y=\dfrac{9.2}{\dfrac{5.6}{28}}=46\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow46n=46\\ \Leftrightarrow n=1\)
\(Vậy:CTHH:C_2H_6O\)

Tỉ lệ về thể tích cũng bằng tỉ lệ về số mol
Ta giả sử :
Khi đốt 1 mol khí X cần 6,5 mol $O_2$ thu được 5 mol $CO_2$ và 5 mol hơi $H_2O$
Bảo toàn nguyên tố với C, H và O :
$n_C = n_{CO_2} = 5(mol); n_H = 2n_{H_2O} = 10(mol)$
$n_O = 2n_{CO_2} + n_{H_2O} - 2n_{O_2} = 2(mol)$
$n_C : n_H : n_O = 5 : 10 : 2$
$\Rightarrow$ CTPT : $C_5H_{10}O_2$
(Không tồn tại CTCT X thoả mãn ở dạng khí)

Đáp án B
Đặt CTPT của X là CxHyOz
Do ở cùng điều kiện nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol.
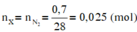
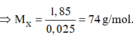

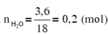
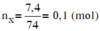
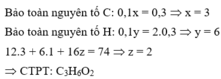

nCO2 = \(\dfrac{1,32}{44}\)=0,03 mol , nH2O =\(\dfrac{1,08}{18}\)=0,06 mol
mC = nCO2.12 = 0,03.12 = 0,36 gam , mH= 2nH2O.1 = 0,06.2 = 0,12 gam
=> mC + mH = 0,36 + 0,12 = 0,48 <=> X chỉ chứa C và H
Gọi CTĐGN của X là CxHy <=> CTPT của X là (CxHy)n
x:y = nC : nH = 0,03 : 0,12 = 1:4 => CTĐGN là CH4
Thể tích của 0,48 gam X = thể tích 0,96 gam O2 ( ở cùng đk to,p) thì số mol của 0,48 gam X cũng bằng mol của 0,96 gam O2 = 0,03 mol
=>Mx=\(\dfrac{0,48}{0,03}\)=16 => n =1 <=> CTPT X là CH4
Ta có: \(n_{Y\left(29,12g\right)}=n_{CO_2}=\dfrac{14,08}{44}=0,32\left(mol\right)\)
\(\Rightarrow M_Y=\dfrac{29,12}{0,32}=91\left(g/mol\right)\)
Gọi CTPT của Y là CxHyOzNt.
\(\Rightarrow x:y:z:t=\dfrac{14,4}{12}:\dfrac{3,6}{1}:\dfrac{12,8}{18}:\dfrac{5,6}{14}=1,2:3,6:0,8:0,4=3:9:2:1\)
\(\Rightarrow\) CTĐGN của Y là (C3H9O2N)n (n nguyên dương)
\(\Rightarrow n=\dfrac{91}{12.3+9+16.2+14}=1\left(tm\right)\)
Vậy: CTPT của Y là C3H9O2N.