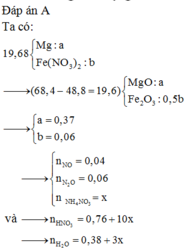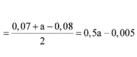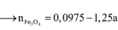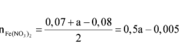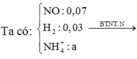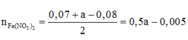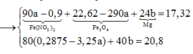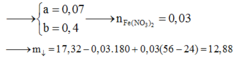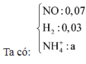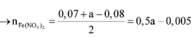Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đọc quá trình - viết sơ đồ → quan sát:
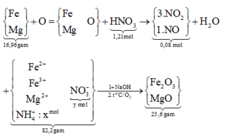
giải hệ Fe, Mg với giả thiết đầu cuối có nFe = 0,2 mol và nMg = 0,24 mol.
gọi x, y như trên. bảo toàn N có: x + y + (0,02 + 0,06 × 2) = 1,21 mol.
Khối lượng muối: mmuối = 82,2 gam = 18x + 62y + 16,96.
Giải hệ được x = 0,025 mol và y = 1,045 mol.
biết x, y
→ giải hệ dung dịch Y có nFe2+ = 0,06 mol và nFe3+ = 0,14 mol.
Mặt khác, bảo toàn electron lại có: nHNO3 phản ứng = 10nNH4+ + 10nN2O + 4nNO + 2nOtrong oxit
→ nO trong oxit = 0,14 mol
→ mX = 19,2 gam. Theo đó, mdung dịch Y = 257,96 gam.
→ Yêu cầu C%Fe(NO3)3 trong Y = 0,14 × 242 ÷ 257,96 ≈ 13,13%.
Đáp án B

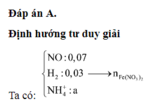
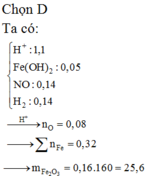
Chọn đáp án A.
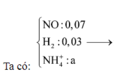
Khí trong Z hóa nâu ngoài không khí là NO.
M Z = 4 , 5 . 4 = 18 < M NO => Khí còn lại có PTK < 18 => Khí đó là H2.

Đặt số mol của Mg, Al, ZnO lần lượt là x, y, z
Có khí H2 thoát ra nên sau phản ứng số mol Fe2+ không đổi.