Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
S là đơn chất vừa có tính khử vừa có tính oxi hoá => (1) – (c)
SO2 là hợp chất vừa có tính oxi hoá vừa có tính khử => (2) – (d)
H2S là hợp chất chỉ có tính khử => (3) – (b)
H2SO4 là hợp chất có tính axit và tính oxi hoá mạnh => (40) – (a)

D đúng.
Cl20 + 2e → 2Cl- ⇒ Cl2 là chất oxi hóa
S2- → S+6 + 8e ⇒ S là chất khử

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
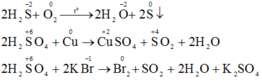

F trong phân tử F2 có số oxi hóa là 0, có khả năng nhận 1 e để chuyển sang trạng thái oxi hóa -1 → tính oxi hóa.
Đáp án: A

Số chất và ion có cả tính oxi hóa và tính khử là: S, FeO, SO2, N2, HCl. Có 5 chất. Đáp án B.
A với c: S có cả tính khử và tính oxi hóa
B với d: SO2 là chất khí có tính oxi hóa và tính khử
C với b: H2S chỉ có tính khử
D với a: H2SO4 chỉ có tính oxi hóa