Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ba phản ứng trong đó CO thể hiện tính khử:
2CO + O 2 → t ° 2 C O 2
+2 -4
3CO + F e 2 O 3 → t ° 2Fe + 3 C O 2
+2 +4
CO + C l 2 → t ° , x t C O C l 4
+2 +4
Ba phản ứng trong đó có C O 2 thể hiện tính oxi hóa:
C O 2 + C → t ° 2CO
+4 +2
C O 2 + 2Mg → t ° 2MgO + C
+4 0
C O 2 + Zn → t ° ZnO + CO
+4 +2

Chọn đáp án B.
6 F e + 2 S O 4 + K 2 C r 2 + 6 O 7 + 7 H 2 S O 4 → 3 F e 2 + 3 S O 4 3 + C r 2 + 2 S O 4 3 + K 2 S O 4 + 7 H 2 O
Dựa vào phản ứng trên ta thấy, Fe tăng từ mức oxi hóa +2 lên +3 và Cr giảm từ mức oxi hóa +6 xuống +3 nên FeSO4 là chất khử, K2Cr2O7 là chất oxi hóa.

Bài 2:
\(m_{HF}=\dfrac{2,5.40\%}{100\%}=1(kg)\\ \Rightarrow n_{HF}=\dfrac{1}{20}=0,05(kmol)\\ PTHH:CaF+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF}=0,025(kmol)\\ \Rightarrow m_{CaF}=0,025.78=1,95(kg)\)
Bài 3:
\(a,\) Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow \begin{cases} 56x+27y=11\\ x+1,5y=0,4 \end{cases} \Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases} \)
\(b,\Sigma n_{HCl}=3n_{Al}+2n_{Fe}=0,2+0,6=0,7(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,7}{2}=0,35(l)\)

Câu 5:
\(n_{Cl_2}=\dfrac{1120}{22,4}=50(mol)\\ PTHH:2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\\ \Rightarrow n_{KMnO_4}=\dfrac{2}{5}n_{Cl_2}=20(mol)\\ \Rightarrow m_{KMnO_4}=20.158=3160(g)\)
Câu 6:
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=10,2(1)\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow x+1,5y=0,5(2)\\ (1)(2)\Rightarrow x=y=0,2(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{10,2}.100\%=52,94\%\\ \Rightarrow \%_{Mg}=100\%-52,94\%=47,06\%\\ b,\Sigma n_{HCl}=3y+2x=1(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{1}{2}=0,5(l)\)
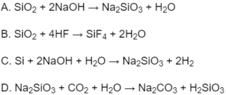
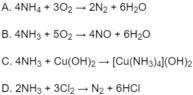
Đáp án A
Các phản ứng xảy ra là:
CO2+ Ba(OH)2 → BaCO3+ H2O (1)
SO2+ Ba(OH)2 → BaSO3+ H2O (2)
4NO2+2 Ba(OH)2 → Ba(NO3)2+ Ba(NO2)2+ 2H2O (3)
2Cl2+2 Ba(OH)2 → BaCl2+ Ba(ClO)2+ 2H2O (4)
H2S+ Ba(OH)2 → BaS + 2H2O (5)
Có 5 phản ứng xảy ra, trong đó phản ứng 3 và 4 là phản ứng oxi hóa khử
Chú ý SiO2 chỉ tan trong kiềm đặc nóng.