Dung dịch B chứa hai chất tan là H2SO4 và Cu(NO3)2. Cho 50ml dung dịch B tác dụng vừa đủ với 31,25ml dung dịch NaOH 16% (d=l,12g/ml), sau phản ứng đem nung kết tủa ở nhiệt độ cao tới khối lượng không đổi thu được 1,6 gam chất rắn. Mặt khác, cho 50 ml dung dịch B tác dụng 2,4 gam Cu thì sau khí phản ứng hoàn toàn giải phóng khí duy nhất NO. Tính thể tích NO ở đktc.
A. 2,24 lít
B. 0,56 lít
C. 0,896 lít
D. 1,12 lít

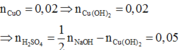
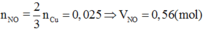
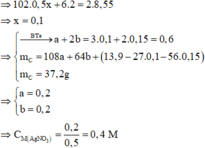

Đáp án B
mNaOH = v.d.C% = 31,25.1,12.16% = 5,6 (gam)
Þ nNaOH = 0,14
Các phản ứng xảy ra theo thứ tự:
2NaOH + H2SO4 g Na2SO4 + 2H2O
Cu(NO3)2 + 2NaOH g Cu(OH)2¯ + 2NaNO3
Cu(OH)2 g CuO + H2O
Do đó trong 50ml dung dịch B chứa 0,05 mol H2SO4 và 0,02 mol Cu(NO3)2 .
Khi cho 50ml dung dịch B tác dụng với 0,0375 mol Cu thì:
3Cu+4H2SO4+Cu(NO3)2g4CuSO4+2NO+4H2O
Do đó