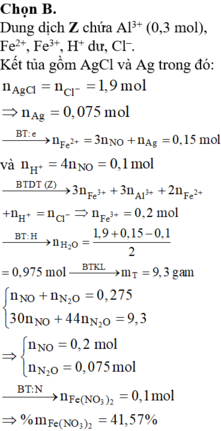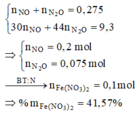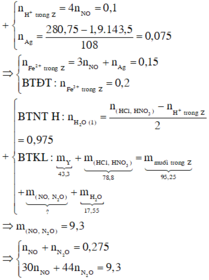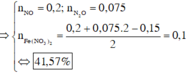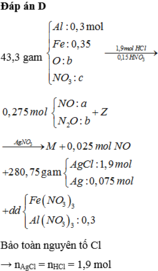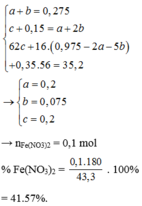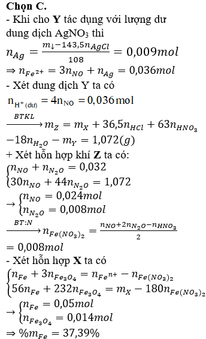Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
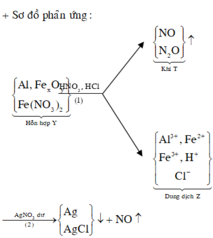
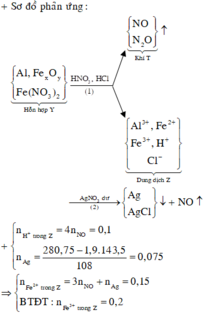
Sơ đồ 1:
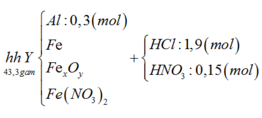
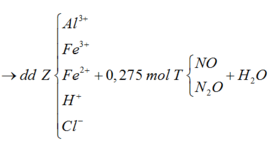
Sơ đồ 2:
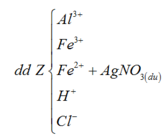
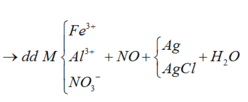
Từ sơ đồ 2 ta có:
BTNT Cl à số mol AgCl = 1,9 (mol) à Số mol Ag = 0,075 (mol)
Số mol H+ dư trong Z = 4nNO = 0,1 (mol)
Bảo toàn e ta có số mol Fe2+ (trong Z) = 3nNO + nAg = 0,15 (mol)
Bảo toàn điện tích cho dung dịch Z ta có: Số mol Fe3+ = 0,2 (mol)
Từ sơ đồ 1 ta có:
Số mol H2O = 1 , 9 + 0 , 15 - 0 , 1 2 = 0 , 975 ( m o l )
BTKL ta có: mkhí T = 9,3 (gam) à n N O + n H 2 O = 0 , 275 30 n N O + 44 n N 2 O = 9 , 3 → n N O = 0 , 2 n N 2 O = 0 , 075
BTNT (N) ta có số mol Fe(NO3)2 = 0 , 2 + 0 , 075 . 2 - 0 , 15 2 = 0 , 1 ( m o l )
à %m(Fe(NO3)2 = 180 . 0 , 1 43 , 3 . 100 % = 41 , 57 %

Đáp án B
+ Dung dịch Z phản ứng với dung dịch AgNO3 dư thu được khí NO, chứng tỏ trong Z có Fe2+, H+ và không còn NO 3 -


Số mol Al là: ![]()
Trộn Al và X không có phản ứng hóa học xảy ra ![]()
*Xét giai đoạn dung dịch Z tác dụng với AgNO3 dư:
Dung dịch Z tác dụng với AgNO3 thu được khí NO => Z chứa Fe2+ và H+ (*)
Z chứa Fe2+ và H+ => Z không chứa N O 3 - (**)
Từ (*) và (**) => Dung dịch Z gồm: ![]()
Các phản ứng tạo kết tủa:
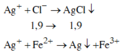
=> Kết tủa: 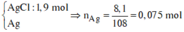
Các quá trình nhường, nhận electron:
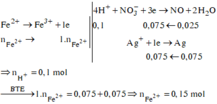
![]()
![]()
![]()
![]()
*Xét giai đoạn Y tác dụng với dung dịch HCl, HNO3:
Sơ đồ phản ứng:
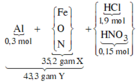
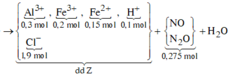
![]()
![]()
![]()
![]()
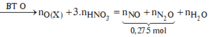
![]()
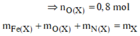
![]()
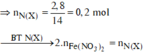
![]()
![]()
Đáp án B.

Đáp án : B
Z + AgNO3 -> NO => H+ dư , NO3- hết ; Z có Fe2+
Kết tủa gồm : nAgCl = nHCl = 1,9 mol => nAg = 0,075 mol
Bảo toàn e : nFe2+ = 3nNO + nAg = 0,15 mol
, nH+ dư = 4nNO = 0,1 mol
Trong dung dịch Z gồm : Al3+ ; Fe2+ ; Fe3+ ; H+ ; Cl-
Bảo toàn điện tích : nAl + 2nFe2+ + 3nFe+ + nH+ = nCl- => nFe3+ = 0,2 mol
=> nFe (Y) = 0,35 mol
Bảo toàn H : nH2O = ½ nH+ pứ = 0,975 mol
Bảo toàn O : nO(Y) + nHNO3 = nO(T) + nH2O
=> nO(Y) = 0,8 mol
Ta có : mY = mAl + mnguyên tố Fe + mO + mN
=> nN = 0,2 mol => nFe(NO3)2 = 0,1 mol
=> %mFe(NO3)2 = 41,57%

Đáp án C
- Thêm AgNO3 vào Y thấy tạo thêm NO chứng tỏ Y chứa Fe2+, H+ dư và không còn NO3-
=> Y + AgNO3 có phản ứng:
Ag+ + Cl- → AgCl
Ag+ + Fe2+ → Ag + Fe3+
Bảo toàn nguyên tố Cl: nAgCl = nCl = 0,3 mol
Có: mtủa = mAg + mAgCl => mAg = 44,022 – 143,5.0,3 = 0,972 g
=> nAg = 0,009 mol
Bảo toàn electron: nFe2+ = 3nNO + nAg = 3.0,009 + 0,009 = 0,036 mol
nH+ dư = 4nNO = 0,036 mol
Vậy dung dịch Y chứa Fe2+(0,036 mol) ; H+ (0,036 mol) ; Cl- (0,3 mol) và Fe3+
Bảo toàn điện tích: 2nFe2+ + 3nFe3+ + nH+ = nCl- => nFe3+ = 0,064 mol
Đặt số mol Fe, Fe3O4, Fe(NO3)2 lần lượt là a, b, c.
Có: mX = 56a + 232b + 180c = 7,488 (1)
Bảo toàn Fe: nFe = a + 3b + c = nFe2+ + nFe3+ = 0,1 mol(2)
nH+ pứ = nHCl bđ + nHNO3 – nH+(Y) = 0,3 + 0,024 – 0,036 = 0,288 mol
Bảo toàn H: nH2O = ½ nH+ pứ = 0,144 mol
Bảo toàn O: 4nFe3O4 + 6nFe(NO3)2 + 3nHNO3 = nH2O + nNO + nN2O
=> 4b + 6c = 0,104 mol(3)
Từ (1,2,3) => a = 0,05 ; b = 0,014 ; c = 0,008
=> %mFe = 56.0,05/7,488 = 37,4% (Gần nhất với giá trị 37,8%)