Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài tập 11)
Mol Al = 0,2 , Mol Fe203 = 0,03 ((O,2 /2 )> ( 0,03))
2Al + Fe2O3 --> Al2O3 + 2 Fe
T 0,2 0,03
P 0,06 0,03 0,03 0,06
S 0,14 0 0,03 0,06
Vậy : Al dư, Al203, Fe
m = 014.27 + 0,03.102 + 0,06.56= 10,2
bài 12
R2CO3 + BaCl2 -> BaCO3 + 2RCl
nBaCl2 = nBaCO3 = 0,2
Bảo toàn khối lượng m = 24,4 + 0,2.208 – 39,4 = 26,6

Đáp án B
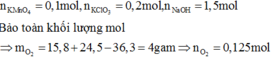
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
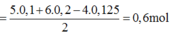


Đáp án B
Xét giai đoạn A tác dụng với H2SO4 đặc, nóng, dư:
Số mol SO2 thu được là: n SO 2 = 0 , 15 mol
Qui đổi hỗn hợp A thành Fe : a mol; O : b mol
![]()
Sơ đồ phản ứng :
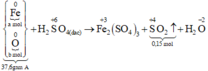
Các quá trình nhường, nhận electron:
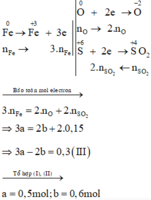
Xét giai đoạn để m gam Fe ngoài không khí:
Sơ đồ phản ứng :


\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_S=\dfrac{3,52}{32}=0,11\left(mol\right)\)
PTHH: Fe + S --to--> FeS
LTL: 0,1 < 0,11 => S dư
Theo pthh: nS (pư) = nFeS = nFe = 0,1 (mol)
Chất rắn Z còn lại là S: nS = 0,11 - 0,1 = 0,01 (mol)
PTHH: 2Al + 3S --to--> Al2S3
0,015<-0,01
=> m = 0,015.27 = 0,405 (g)
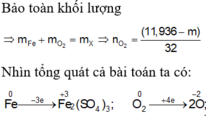
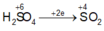
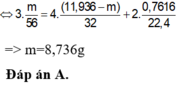

2Al +Fe2O3---.2Fe +Al2O3
Ta có
n\(_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\)
n\(_{Fe2O3}=\frac{12}{160}=0,075\left(mol\right)\)
=>Al dư
Theo pthh
n\(_{Fe}=2n_{Fe2O3}=0,15\left(mol\right)\)
=>m\(_{Fe}=0,15.56=8,4\left(g\right)\)
Theo pthh
n\(_{Al2O3}=n_{Fe2O3}=0,075\left(mol\right)\)
m\(_{Al2O3}=0,075.102=7,65\left(g\right)\)
Theo pthh
n\(_{Al}=2n_{Fe2O3}=0,15\left(mol\right)\)
m\(_{Al}=0,15.27=4,05\left(g\right)\)
m\(_{Al}dư=5,04-4,05=0,99\left(g\right)\)
m=0,99+7,65+8,4=17,04(g)
Chúc bạn học tốt