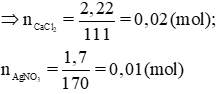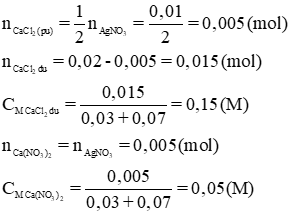Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) dung dịch xuất hiện kết tủa trắng ( AgCl )
CaCl2 + 2AgNO3 --> Ca(NO3)2 + 2AgCl
b)
CaCl2 + 2AgNO3 --> Ca(NO3)2 + 2AgCl
Tpu 0.02 0.01
Pu 0.005 0.01 0.01 0.02
Spu 0.015 0.01 0.02
n CaCl2= m/M= 2.22/ 111= 0.02 (mol)
n AgNO3= 1.7 / 170= 0.01 (mol)
Ta có: 0.02/ 1 > 0.01/ 2 => CaCl2 dư, AgNO3 hết
m AgCl = 0.02 * 143.5 = 2.87 (g) => m kết tủa = 2.87 g
c) Tổng thể tích 2 dung dịch là:
V = 0.03 + 0.07= 0.1 ( lít )
Nồng độ mol của dung dịch CaCl dư:
CM ( CaCl2 ) = 0.015/ 0.1 = 0.15 M
Nồng độ mol của dung dịch Ca(NO3) tạo thành sau phản ứng là:
CM [ Ca(NO3)2 ] = 0.01/ 0.1 = 0.1 M

Phương trình phản ứng
CaCl2 (dd) + 2AgNO3 -> 2AgCl (r ) + Ca(NO3)2 (dd)
a) Hiện tượng quan sát được: Tạo ra chất không tan, màu trắng, lắng dần xuống đáy cốc đó là AgCl
b) Đáp số
mAgCl=1,435 gam
c) Trong 30 + 70 = 100 (ml) dd sau phản ứng có chứa 0,02 – 0,05 =0,015 (mol) CaCl2 dư và 0,005 mol Ca(NO3)2
Do vậy ta có
CMCaCl2=0,15M và CMCa(NO3)2 = 0,05 M.
a) Phương trình phản ứng CaCl2(dd) + 2AgNO3 → 2AgCl (r) + Ca(NO3)2 (dd)
Hiện tượng quan sát được: Tạo ra chất không tan, màu trắng, lắng dần xuống đáy cốc đó là AgCl
b) MCaCl2 = 40 + 35,5. 2 = 111g/mol ; MAgNO3 = 108 + 14 + 16.3 = 170g / mol
Tỉ lệ mol: 0,02/1 > 0,01/2 ⇒ AgNO3 phản ứng hết, CaCl2 dư.
Theo pt: nAgCl = nAgNO3 = 0,01 (mol) ⇒ mAgCl = 0,01. 143,5 = 1,435 (g)
c) Chất còn lại sau phản ứng: Ca(NO3)2 và CaCl2 dư
Theo pt:

a , Xuất hiện kết tủa màu trắng
PTHH : NaCl + AgNO3 -> NaNO3 + AgCl\(\downarrow\)
b , nNaCl = 0,02 (mol) , nAgNO3 = 0,01 (mol) => NaCl dư 0,01 (mol)
mAgCl = 0,01 . 143,5=1,435 (g)
c , Vdung dịch = 0,12 (l)
CM (NaCl) = 0,01/0,12=1/12(M) =CM(NaNO3)