Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nhiệt lượng tỏa ra
Q A l = m A l . C A l ( t − 1 ) = 9900 J Q t o a = Q t h u Q H 2 O = Q t o a = 9900 J → 9900 = m H 2 O . C H 2 O ( t − t 2 ) → 9900 = m H 2 O .4200 ( 25 − 20 ) → m H 2 O = 0 , 47 k g
Đáp án: A

Ta có:
Nhiệt lượng do quả cầu bằng nhôm tỏa ra:
Q 1 = m A l . c A l . t 1 − t = 0 , 105.880. 142 − 42 = 9240 J
Nhiệt lượng do nước thu vào là:
Q 2 = m H 2 O . c H 2 O t − t 2 = m H 2 O .4200. 42 − 20 = 92400 m H 2 O
Theo phương trình cân bằng nhiệt ta có:
Q 1 = Q 2 ⇔ 9240 = 92400 m H 2 O ⇒ m H 2 O = 0 , 1 k g = 100 g
Đáp án: B

Đáp án D
Nhiệt lượng tỏa ra :
QAl = mAl.CAl (t1 − t) = 28600 J
Theo điều kiện cân bằng nhiệt:
Qtỏa = Qthu → QH2O = Qtỏa = 28600 J
→ 28600 = mH2O.CH2O(t − t2 )
→ 28600 = mH2O. 4200 ( 35 − 20 )
→ mH2O = 0,454 kg

Nhiệt lượng tỏa ra :
Q A l = m A l .C A l ( t 1 – t ) = 9900 J
Theo điều kiện cân bằng nhiệt :
Q t ỏ a = Q t h u . Q H 2 O = Q t ỏ a = 9900 J
⇒ 9900 = m H 2 O .C H 2 O (t – t 2 )
⇒ 9900 = m H 2 O . 4200 ( 25 – 20 )
⇒ m H 2 O = 0,47 kg

Đáp án D
Nhiệt lượng tỏa ra : QAl = mAl.CAl ( t1 – t ) = 28600 J
Theo điều kiện cân bằng nhiệt : Qtoả = Qthu => QH2O = Qtỏa = 28600 J
=> 28600 = mH2O.CH2O(t – t2 ) => 28600 = mH2O. 4200 ( 35 – 20 )
=> mH2O = 0,454 kg

Ta có:
Qtoa là nhiệt lượng mà sắt tỏa ra
Qthu là nhiệt lượng mà nước và nhôm nhận được để tăng nhiệt độ lên 800C và nhiệt lượng của 5g nước tăng từ 200C lên 1000C rồi hóa hơi
Khi quả cầu bắt đầu chạm vào m1=5g nước đã bốc hơi nên lượng nước tăng từ 200C lên 800C chỉ có
m′ = 100 − 5 = 95g
+ Q t o a = m F e c F e t - 80
+ Q t h u = m A l c A l 80 - 20 + m ' c n c 80 - 20 + m 1 c n c 100 - 20 + m 1 L
Theo phương trình cân bằng nhiệt, ta có:
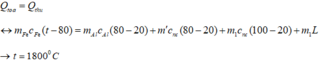
Đáp án: A


\(m_nc_n\left(25-20\right)=m_{Al}c_{Al}\left(100-25\right)\)
=> \(m_n.4200.5=0,15.880.75\)
=> mn = 33/70 \(\approx0,47kg\)
camr ơn bạn nhiều nha :<