Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
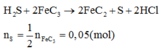
Chú ý: Không tồn tại muối sunfua của Al và Fe(III). H2S không phản ứng với AlCl3 nhưng nếu
![]()
Có sự khác nhau này do Fe3+ có tính oxi hóa mạnh còn Al3+ tính oxi hóa yếu

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng. Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
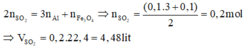

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng.Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
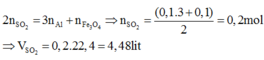

Ta có pthh:
\(Fe+S\underrightarrow{t^o}FeS\left(1\right)\)
x1 x1 x1 (mol)
Sau khi nung trong hỗn hợp A có :
\(\left(x-x_1\right)molS\)
\(\left(2x-x_1\right)molFe\)
và x1 mol FeS
- hòa tan A trong axit HCl dư :
\(Fe+2HCl\rightarrow FeCL_2+H_2\uparrow\left(2\right)\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\left(3\right)\)
Còn lại 0,4 g chất rắn B là lưu huỳnh dư
\(nS=x-x_1=\dfrac{0,4}{32}=0,0125\left(mol\right)\left(I\right)\)
Dung dịch C gồm HCl dư và FeCl2 với số mol là 2x .
Khí D gồm H2 và H2S .
Sục khí D từ từ vào dung dịch CuCl2 dư , chỉ có H2S phản ứng.
\(CuCl_2+H_2S\rightarrow CuS\downarrow+2HCl\left(4\right)\)
Kết tủa đen tạo thành là CuS
theo (1) (2) , (4) :
\(nCuS=x_1=\dfrac{4,8}{96}=0,05\left(mol\right)\left(II\right)\)
Kết hợp (I) ; và (II) ta có : x - x1= 0,0125
x = 0,0125 + 0,05 = 0,0625
Hiệu suất pứ tạo thành hh A:
Theo S: \(h\%=\dfrac{0,05}{0,0625}.100\%=80\%\)

Đáp án B.
Gọi nCu = y, nFe = x mol

Áp dụng định luật bảo toàn e ta có: 3x+2y = 0,07 (1)
Khối lượng hai kim loại = 1,84 g: 56x+64y = 1,84 (2).
Giải 1,2 ta có: x = 0,01, y = 0,02 (mol)

`Fe + 2HCl -> FeCl_2 + H_2 ↑`
`0,2` `0,2` `(mol)`
`FeS + 2HCl -> FeCl_2 + H_2 S↑`
`0,1` `0,1` `(mol)`
`H_2 S + Pb(NO_3)_2 -> PbS↓ + 2HNO_3`
`0,1` `0,1` `(mol)`
`n_[PbS] = [ 23,9 ] / 239 = 0,1 (mol)`
`n_Y = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
`a)` Hỗn hợp `Y` gồm khí `H_2` và `H_2 S`
`=> n_[H_2 S] = 0,1 (mol)`
`=> n_[H_2] = 0,3 - 0,1 = 0,2 (mol)`
`b)m_[hh] = 0,2 . 56 + 0,1 . 88 = 20 (g)`



Đáp án C