Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
- Phần trăm của đồng vị còn lại là 100% - 54,5% = 45,5%
- Công thức tính nguyên tử khối trung bình:
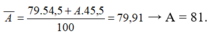

\(\overline{NTK}_{Li}=6,07\\ \Leftrightarrow\dfrac{7.18,9\%+A_2.\left(100\%-18,9\%\right)}{100\%}=6,07\\ \Leftrightarrow A_2=5,85\)

a), Đặt đồng vị thứ 2 của đồng là A2.
\(\overline{NTK}_{Cu}=63,54\\ \Leftrightarrow\dfrac{63.73\%+A_2.27\%}{100\%}=63,54\\ \Leftrightarrow A_2=65\left(đ.v.C\right)\)
b, Khi có 81 nguyên tử đồng vị thứ 2 thì số nguyên tử 63Cu là:
\(\dfrac{81.73}{27}=219\left(nguyên.tử\right)\)
c) Phần trăm khối lượng đồng vị 63Cu có trong phân tử Cu2O là:
\(73\%.\dfrac{63,54.2}{63,54.2+16}\approx64,837\%\)

Câu 1:
Đặt đồng vị thứ hai là: \(^a_{51}Sb\)
\(\Rightarrow\%_{^aSb}=100\%-62\%=38\%\)
Mà \(\overline{A}=121,76\)
\(\Leftrightarrow\dfrac{121.62+a.38}{100}=121,76\)
\(\Rightarrow a=123\)
Vậy nguyên tử khối của đồng vị thứ hai mà 123
Kí hiệu: \(^{123}_{51}Sb\)

Ta có: \(\overline{M}=\dfrac{63.73+x.\left(100-73\right)}{100}\Leftrightarrow x=\dfrac{100.63,54-63.73}{100-73}=65\)
Đồng vị thứ hai là \(^{65}_{29}Cu\)
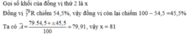
bạn ơi đề thiếu rồi : đề phải cho biết \(Antimon\left(sb\right)\) có 2 đồng vị như thế nào chứ bạn . VD như : đồng có 2 đồng vị là \(\dfrac{63}{29}cu\) và \(\dfrac{65}{29}cu\)