Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nanken = nankan = nBr2 = 0,1 mol.
Số nguyên tử C của ankan và anken như nhau = nCO2 : nhh khí = 0,6 : 0,2 = 3 → C3H6 và C3H8

nBr2 phản ứng = 80.20% : 160 = 0,1 = nAnken
⇒ n Ankan = nAnken = 0,1
Đốt cháy hoàn toàn m gam hỗn hợp đó thu được 0,6 mol CO2
mà Ankan và Anken đều có cùng số C
⇒ số C trong Ankan hoặc Anken là : 0,6 : 0,1 : 2 =3
Đáp án C.

Đáp án A
Trong Y: nX = 0,35 mol; nH2 = 0,07 mol → Trong X: nC2H4 = 0,25 và nC3H6 = 0,1.
- Vì tỉ lệ mol của hai ankan bằng tỉ lệ mol của 2 anken tương ứng ban đầu; mặt khác anken, hiđro tham gia phản ứng và ankan tạo ra đều với số mol như nhau
→ hhZ có 0,07 mol ankan và 0,35 - 0,07 = 0,28 mol anken dư, trong đó:
nC3H6 = 0,7143 x 0,28 = 0,2
→ nC2H4 = 0,02.
nC3H8 = 0,7143 x 0,07 = 0,05
→ nC2H6 = 0,02

$n_{CO_2} = 0,5(mol) ; n_{H_2O} = 0,5625(mol)$
$\Rightarrow n_A = 0,5625 - 0,5 = 0,0625(mol)$
$\Rightarrow n_B = 0,3 - 0,0625 = 0,2375(mol)$
Bảo toàn C :
$0,0625.C_A + 0,2375.C_B = 0,5$
Không có số nguyên $C_A,C_B$ nào thỏa mãn
cho mình hỏi là nH2O=0.5625 vậy?? sao mình tính ra 0.7 mol???

Đáp án A
Áp dụng định luật bảo toàn nguyên tố:
![]()
Khi cho T qua dung dịch nước brom thì C2H4, C2H4, C4H8, C4H6 phản ứng với brom.
![]() (1)
(1)
![]() (2)
(2)
Từ (1) và (2) có
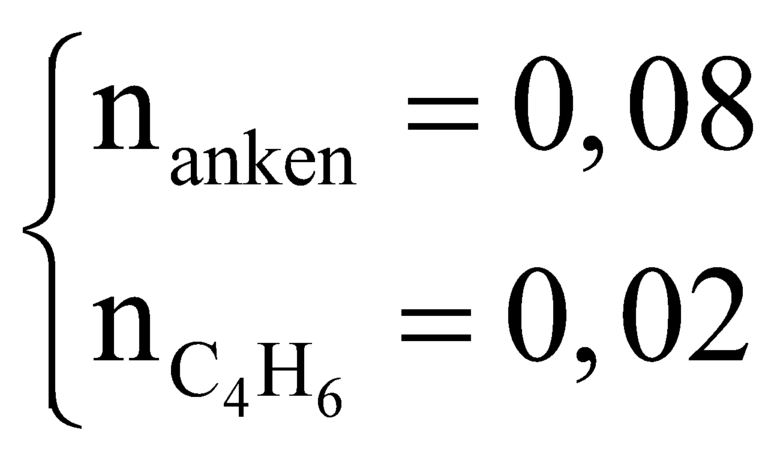
![]()

Đặt :
nX = nY = x (mol)
CT : CnH2n+2 , CmH2m+2
nCO2 = 13.44/22.4 = 0.6 (mol)
BT C :
x(n+m) = 0.6 (1)
mhh = x(14n + 2) + x(14m + 2) = 8.8
=> 14x(n+m) + 4x = 8.8
=> 14*0.6 + 4x = 8.8
=> x = 0.1
Từ (1) => n + m = 0.6/0.1 = 6
BL : n = 2 , m = 4 => C2H6 , C4H8
n = 1 , m = 5 => CH4 , C5H12

Đáp án A
Hướng dẫn
CnH2n + 3n/2O2 → nCO2 + nH2O
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O nankan = 0,23 – 0,14 = 0,09 mol
=> nanken = 0,1 – 0,09 = 0,01 mol
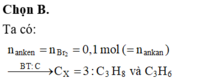
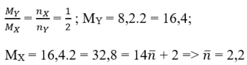
mBr2 = 120.20/100 = 24g nBr2 = 0,15 mol =>nankan = nanken = nBr2 = 0,15 mol
Gọi CTPT của ankan và anken là CnH2n+2 và CnH2n
=>nCO2 = 0,15n + 0,15n = 20 , 6 22 , 4 ⇒ n = 3
=>Chọn A.