
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(a,Ca+2HCl\rightarrow CaCl_2+H_2\left(1\right)\\ CaO+2HCl\rightarrow CaCl_2+H_2O\left(2\right)\\ Đặt:n_{Ca}=a\left(mol\right);n_{CaO}=b\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}111a+111b=22,2\\22,4a=2,24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \Rightarrow\%m_{CaO}=\dfrac{0,1.56}{0,1.56+0,1.40}.100\approx52,83\%\\ \Rightarrow\%m_{Ca}=47,17\%\\ b,n_{HCl}=2.\left(a+b\right)=0,4\left(mol\right)\\ \Rightarrow m_{ddHCl}=\dfrac{0,4.36,5.100}{36,5}=40\left(g\right)\)


a.Theo định luật bảo toàn khối lượng, ta có:
\(m_{Cl_2}=36,2-7,8=28,4g\)
\(n_{Cl_2}=\dfrac{m}{M}=\dfrac{28,4}{71}=0,4mol\)
\(2Al+3Cl_2\rightarrow\left(t^o\right)2AlCl_3\)
2 3 2 ( mol )
\(2Mg+Cl_2\rightarrow\left(t^o\right)2MgCl_2\)
2 1 2 ( mol )
Gọi \(n_{Al}=x\)
\(n_{Mg}=y\)
\(\Rightarrow m_{Al}=27x\)
\(\Rightarrow m_{Mg}=24y\)
Ta có:
\(\left\{{}\begin{matrix}m_{hh}=27x+24y=7,8\\\dfrac{3}{2}x+\dfrac{1}{2}y=0,4\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=\dfrac{19}{75}\\y=\dfrac{1}{25}\end{matrix}\right.\)
\(\Rightarrow m_{Al}=27.\dfrac{19}{75}=6,84g\)
\(\Rightarrow m_{Mg}=24.\dfrac{1}{25}=0,96g\)
\(\%m_{Al}=\dfrac{6,84.100}{7.8}=87,7\%\)
\(\%m_{Mg}=100\%-87,7\%=12,3\%\)

\(n_{KClO_3}=\dfrac{73,5}{122,5}=0,6\left(mol\right)\)
\(n_{KCl}=\dfrac{33,5}{74,5}=\dfrac{67}{149}\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
a------------>a
4KClO3 --to--> 3KClO4 + KCl
b-------------------->0,25b
=> \(\left\{{}\begin{matrix}a+b=0,6\\a+0,25b=\dfrac{67}{149}\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=0,39955\left(mol\right)\\b=0,20045\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%_{phân.hủy.theo.\left(a\right)}=\dfrac{0,39955}{0,6}.100\%=66,5917\%\\\%_{phân.hủy.theo.\left(b\right)}=\dfrac{0,20045}{0,6}.100\%=33,4083\%\end{matrix}\right.\)


Bài 29 :
\(n_{CO2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(CaO+2HCl\rightarrow CaCl_2+H_2O|\)
1 2 1 1
0,3 0,6 0,3
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,2 0,4 0,2 0,2
a) \(n_{CaCO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{CaCO3}=0,2.100=20\left(g\right)\)
\(m_{CaO}=36,8-20=16,8\left(g\right)\)
0/0CaO = \(\dfrac{16,8.100}{36,8}=45,65\)0/0
0/0CaCO3 = \(\dfrac{20.100}{36,8}=54,35\)0/0
b) Có : \(m_{CaO}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,6+0,4=1\left(mol\right)\)
\(C_{M_{ddHCl}}=\dfrac{1}{5}=0,2\left(M\right)\)
\(n_{CaCl2\left(tổng\right)}=0,3+0,2=0,5\left(mol\right)\)
\(C_{M_{CaCl2}}=\dfrac{0,5}{5}=0,1\left(M\right)\)
Chúc bạn học tốt
Bài 28:
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\\ K_2CO_3+2HCl\rightarrow2KCl+CO_2+H_2O\\ Đặt:n_{CaCO_3}=a\left(mol\right);n_{K_2CO_3}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}100a+138b=6,76\\a+b=\dfrac{2,64}{44}=0,06\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,02\end{matrix}\right.\\ \%m_{CaCO_3}=\dfrac{0,02.100}{6,76}.100\approx29,586\%\\ \Rightarrow\%m_{K_2CO_3}\approx70,414\%\)

b1 , câu a
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(4Fe+3O_2\underrightarrow{t^o}2Fe_2O_3\)
\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(N_2+O_2\underrightarrow{t^o}2NO\)
\(2CO+O_2\underrightarrow{t^o}2CO_2\)
\(2NO+O_2\underrightarrow{t^o}2NO_2\)
\(2SO_2+O_2\underrightarrow{t^o}2SO_3\)
\(CH_4+O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_5OH+33O_2\underrightarrow{t^o}3CO_2\uparrow+3H_2O\uparrow\)
bài 1 . câu b
\(2KMnO_4\underrightarrow{t^o}KMnO_2+O_2+K_2MnO_4\)
\(2KClO_3\underrightarrow{t^o:500^oC}\left(MnO_2\right)-2KCl+3O_2\)
( MnO2 là chất xúc tác và 500 độ C là đk nhiệt độ để KClO3 tạo ra O2)
\(2H_2O_2\underrightarrow{phanhuy}2H_2O+O_2\uparrow\)
them kiến thức bổ sung nek:
Bình thường H2O2 phân huỷ chậm trong dung dịch ở nhiệt độ thường. Nhưng nếu cho vào dung dịch này một ít bột MnO2, bọt oxi sẽ thoát ra rất mạnh.
vậy theo mình nên cho MnO2 vô thấy cũng được nhưg đề không yêu cầu điều chế oxi mạnh nên thôi.



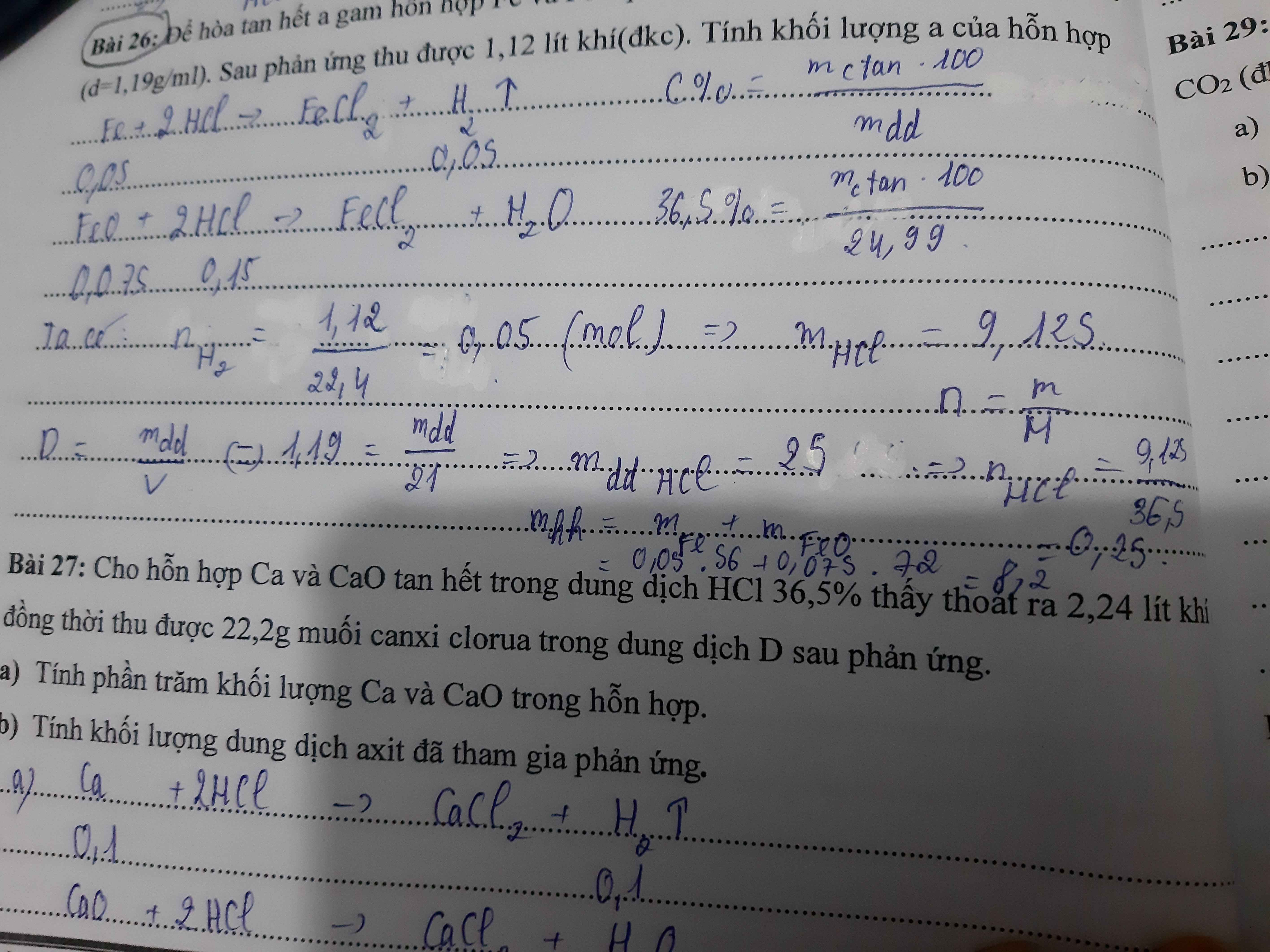

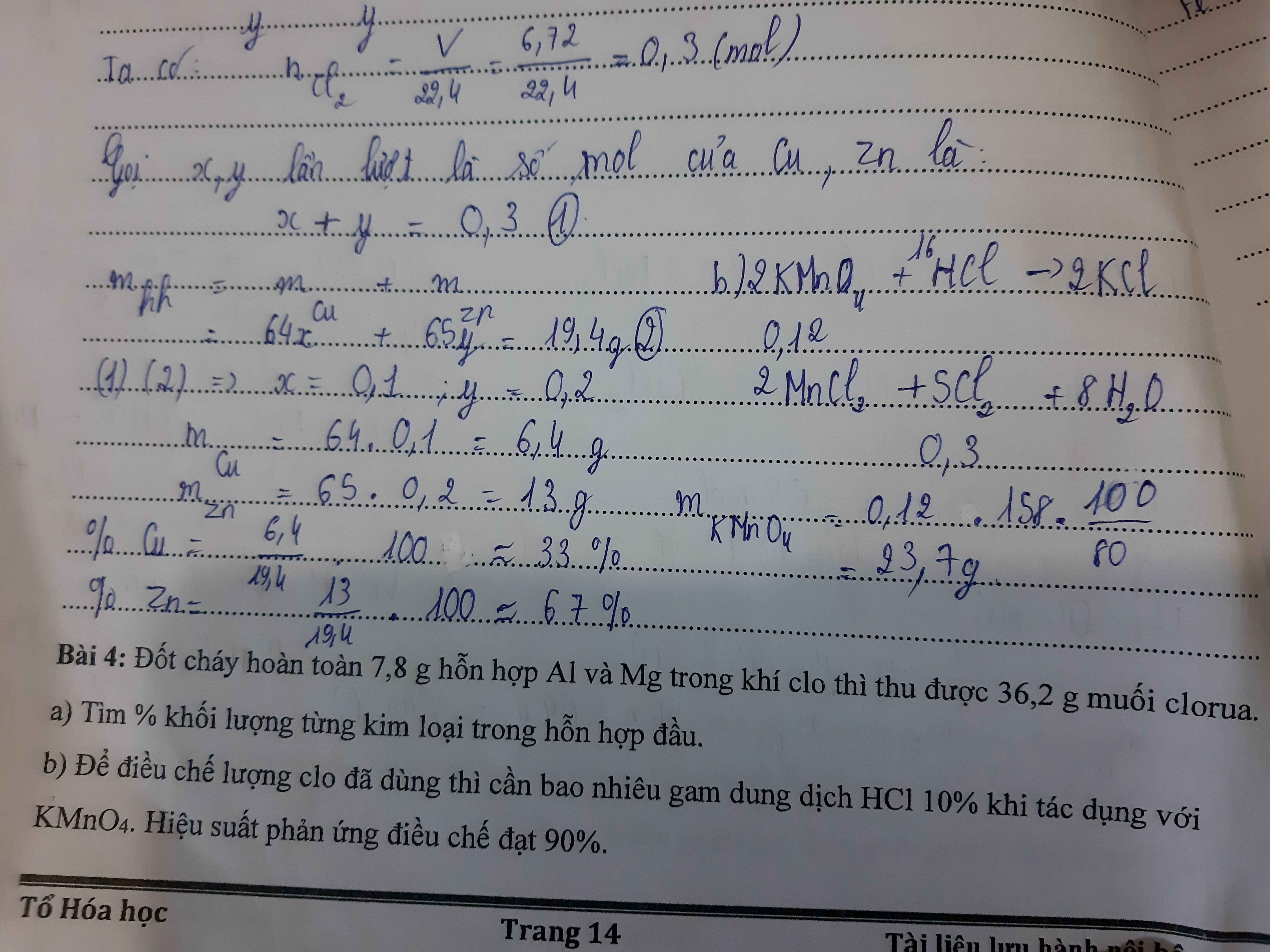







Bài 30:
\(Đặt:n_{KBr}=a\left(mol\right);n_{NaCl}=b\left(mol\right)\left(a,b>0\right)\\ KBr+AgNO_3\rightarrow AgBr\downarrow+KNO_3\\ NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\\ \Rightarrow\left\{{}\begin{matrix}119a+58,5b=23,6\\188a+143,5b=47,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\\ a,m_{KBr}=0,1.119=11,9\left(g\right)\\ m_{NaCl}=0,2.58,5=11,7\left(g\right)\\ b,n_{AgNO_3}=a+b=0,3\left(mol\right)\\ \Rightarrow V_{ddAgNO_3}=\dfrac{0,3}{0,5}=0,6\left(l\right)=600\left(ml\right)\)