Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án D
nCO2 = 0,14 mol ; nH2O = 0,17 mol
Vì các chất đều no => nC2H5OH = nH2O - nCO2 = 0,03 mol
=> naxit + andehit = 0,03 mol
Bảo toàn C : 3naxit + 2nandehit = nCO2 – 2nancol = 0,08 mol
=>naxit = 0,02 ; nandehit = 0,01 mol
=> m = 3,3g
Vậy trong 16,5g X có nandehit = 0,01.5 = 0,05 mol
=> nAg = 2nandehit = 0,1 mol
=> p = 10,8g

Đáp án A.
n C O 2 = 0 , 1 ( m o l ) ; n H 2 O = 0 , 15 ( m o l ) ; n A g = 0 , 12 ( m o l )
Ta có: C ¯ của hỗn hợp M = n C O 2 n M = 1 => A,B,C,D đều có 1 nguyên tử C
Vậy A, B, C, D chỉ có thể lần lượt là: CH4, HCHO, CH3OH, HCOOH.
Gọi số mol tương ứng của A,B,C,D là a,b,c,d (mol)
a + b + c + d = 0 , 1 2 a + b + 2 c + d = n H 2 O = 0 , 15 ⇒ a + c = 0 , 05 b = 0 , 01 d = 0 , 04 4 b + 2 d = n A g = 0 , 12
Vậy % số mol của D là 40%

Đáp án B
n H 2 O = 0 , 48 ( m o l ) ; n C O 2 = 0 , 4 ( m o l ) ; ⇒ n H 2 O > n C O 2 ⇒ a n c o l n o , m ạ c h h ở
Vì axit no, đơn chức, mạch hở nên khi đốt cháy axit hoặc este ta đều thu được
n H 2 O = n C O 2
⇒ n H 2 O - n C O 2 = 0 , 08 ( m o l ) = n a n c o l

Đáp án D
n C O 2 c h á y = 0 , 7 ( m o l ) ; n C O 2 t r o n g p h ả n ứ n g c ộ n g N a H C O 3 = 0 , 5 ( m o l ) ⇒ n C O O H = 0 , 5 ( m o l )
Bảo toàn khối lượng ta có:
m X = m C + m H + m O M à n O t r o n g X = 2 n C O O H = 1 ( m o l ) ⇒ m H t r o n g X = 25 , 3 - 12 . 0 , 7 - 16 . 1 = 0 , 9 ( g ) ⇒ n H t r o n g X = 0 , 9 ( m o l ) = 2 n H 2 O ⇒ n H 2 O = 0 , 45 ( m o l ) ⇒ m H 2 O = 8 , 1 ( g )
Chú ý: Ta có thể giải bài toán theo cách khác. Gọi số mol của mỗi chất trong X lần lượt là x, y, z(mol)
Sau đó ta lập hệ 3 phương trình 3 ẩn dựa vào 3 số liệu của đề bài. Tuy nhiên cách làm này không áp dụng được cho các bài toán có nhiều hơn 3 chất trong hỗn hợp hoặc bài toán không cho rõ công thức các chất.
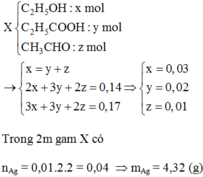
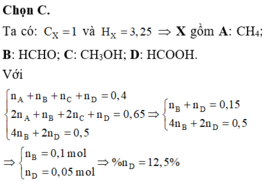
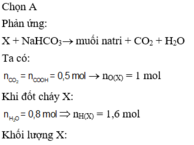
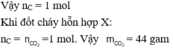

Đáp án D
n C O 2 = 0 , 14 ( m o l ) ; n H 2 O = 0 , 17 ( m o l )
Khi đốt cháy C2H5COOH và CH3CHO đều thu được
Trong 13,2 gam X gọi n C H 3 C H O = x ( m o l ) ;
=> 44x +74.2x+46.3x=13,2(g) =>x=0,04(mol)
Vậy m = 8,64(g)