Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) n X = 4,48/22,4 = 0,2(mol)
Số mol của hidrocacbon có số C lớn hơn(n nguyên tử C) : 0,2.25% = 0,05(mol)
Số mol của hidrocacbon có số C nhỏ hơn(m nguyên tử C) : 0,2 -0,05 = 0,15(mol)
n CO2 = 10,08/22,4 = 0,45(mol)
Bảo toàn nguyên tố với C :
0,05n + 0,15m = 0,45
Với n = 3 ; m = 2 thì thỏa mãn
Vậy hai hidrocacbon là C3H6 và C2H6 hoặc C3H8 và C2H4
b)
- Nếu X gồm C3H6(0,05 mol) và C2H6(0,15 mol) :
$nCH_2=CH-CH_3 \xrightarrow{t^o,p,xt} (-CH_2-CH(CH_3)-)_n$
n polime = 0,05/n(mol)
=> m polime = 42n . 0,05/n = 2,1(gam)
- Nếu X gồm C3H8(0,05 mol) và C2H4(0,15 mol) :
$nCH_2=CH_2 \xrightarrow{t^o} (-CH_2-CH_2-)_n$
n polime = 0,15/n(mol)
=> m polime = 28n.0,15/n = 4,2(gam)

Công thức phân tử của hợp chất A :
Số mol các sản phẩm của phản ứng :
n SO 2 = 0,1 mol; n H 2 O = 0,1 mol
Khối lượng của hiđro có trong 0,1 mol H 2 O (2 g.0,1 = 0,2 g) và khối lượng của lưu huỳnh có trong 0,1 mol SO 2 (32 g.0,1 = 3,2 g) đúng bằng khối lượng của hợp chất A đem đốt (3,4 g).
Vậy thành phần của hợp chất A chỉ có 2 nguyên tố là H và S.
- Tỉ lệ giữa số mol nguyên tử H và số mol nguyên tử S là :
n H : n S = 0,1.2 : 0,1 = 2 : 1
Công thức phân tử của hợp chất A là : H 2 S

Xác định công thức phân tử của hợp chất A
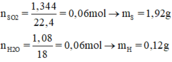
Như vậy hợp chất A chỉ có nguyên tố S và H (Do mS + mH = 1,92 + 0,12 = 2,04 =mA)
Đặt công thức phân tử hợp chất là HxSy
Ta có tỉ lệ x : y = nH : nS = 0,12 : 0,06 = 2 : 1
Vậy công thức phân tử của A và là H2S.

a)
n CO2 = 403,2/1000.22,4 = 0,018(mol)
n H2O = 0,27/18 = 0,015(mol)
Bảo toàn nguyên tố với C,H :
n C = n CO2 = 0,018(mol)
n H = 2n H2O = 0,015.2 = 0,03(mol)
=> n O = (0,486 - 0,018.12 - 0,03.1)/16 = 0,015(mol)
n C : n H : n O = 0,018 : 0,03 : 0,015 = 6 : 10 : 5
=> CTP là (C6H10O5)n
M A = 162n < 170 => n <1,049
=> n = 1
Vậy CTPT của A là C6H10O5
b)
A có 1 -OH và 1 -COOH
CTCT của A : HO-CH2-CH2-COO-CH2-CH2-COOH
B : HO-CH2-CH2-COONa
$HO-CH_2-CH_2-COOCH_2-CH_2-COOH + 2NaOH \to 2HO-CH_2-CH_2-COONa + H_2O$
a)
n CO2 = 403,2/1000.22,4 = 0,018(mol)
n H2O = 0,27/18 = 0,015(mol)
Bảo toàn nguyên tố với C,H :
n C = n CO2 = 0,018(mol)
n H = 2n H2O = 0,015.2 = 0,03(mol)
=> n O = (0,486 - 0,018.12 - 0,03.1)/16 = 0,015(mol)
n C : n H : n O = 0,018 : 0,03 : 0,015 = 6 : 10 : 5
=> CTP là (C6H10O5)n
M A = 162n < 170 => n <1,049
=> n = 1
Vậy CTPT của A là C6H10O5
b)
A có 1 -OH và 1 -COOH
CTCT của A : HO-CH2-CH2-COO-CH2-CH2-COOH
B : HO-CH2-CH2-COONa
HO−CH2−CH2−COOCH2−CH2−COOH+2NaOH→2HO−CH2−CH2−COONa+H2O
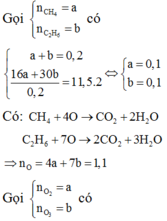
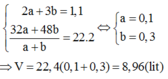
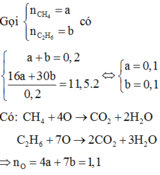
\(\left\{{}\begin{matrix}n_{H2O}=\frac{9}{18}=0,5\left(mol\right)\\n_{CO2}=\frac{8,96}{22,4}=0,4\left(mol\right)\end{matrix}\right.\)
Ta gọi số mol của 2 hidrocacbon là a(mol) và CTPT 2 hidrocacbon là CnHx và CnHy
Áp dụng định luật bảo toàn nguyên tố với C :
\(C_nH_x\rightarrow nCO_2\)
a_________an
\(C_nH_y\rightarrow nCO_2\)
a __________an
\(\Rightarrow n_{CO2}=an+an=2an=0,4\left(mol\right)\Rightarrow a=\frac{0,2}{n}\)
\(C_nH_x\rightarrow\frac{x}{2}H_2O\)
a_________ 0,5ax (mol)
\(C_nH_y\rightarrow\frac{y}{2}H_2O\)
a_______0,5ay (mol)
\(\Rightarrow n_{H2O}=0,5ax+0,5ay=0,5\Rightarrow a=\frac{1}{x+y}\)
\(\Rightarrow\frac{0,2}{n}=\frac{1}{x+y}\)
\(\Rightarrow5n=x+y\)
Biện luận :
Nếu n = 1 thì
- x = 4 ⇒ CT là CH4
- y= 1 ⇒ CT là CH (loại)
Nếu n=2 thì :
+) x = 4 ⇒ CT là C2H4
y = 6 ⇒ CT là C2H6 (chọn)
+) x = 2 ⇒ CT là C2H2
y = 8 ⇒ CT là C2H8 (loại)
Vậy CTPT hai hidrocacbon là C2H4 và C2H6