Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
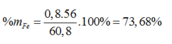

Đáp án D.
Gọi nCu = y, nFe = x mol

Áp dụng định luật bảo toàn e ta có: 3x+2y = 0,7 (1)
Khối lượng hai kim loại = 1,84 g: 56x+64y = 184 (2).
Giải 1,2 ta có: x = 0,1, y = 0,2 (mol)
% m F e = 0 , 1 . 56 18 , 4 . 100 % = 30 , 43 %

a) \(2Fe+6H_2SO_4\text{đặc}\rightarrow^{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2FeO+4H_2SO_4\text{đặc}\rightarrow^{t^0}Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
\(2Fe_3O_4+10H_2SO_4\text{đặc}\rightarrow3Fe_2\left(SO_4\right)_3+SO_2+10H_2O\)
Quy đổi hỗn hợp A gồm x mol Fe và y mol O
\(\Rightarrow56x+16y=49,6\) (1)
\(Fe\rightarrow Fe^{3+}+3e\)
x ------------> 3x
\(S^{+6}+2e\rightarrow S^{+4}\)
..........0,8 <--- 0,4
\(O+2e\rightarrow O^{2-}\)
y --> 2y
\(\Rightarrow3x=2y+0,8\) (2)
Giải hệ (1)(2) được x = 0,7 mol, y = 0,65 mol
\(\Rightarrow\%m_O=\dfrac{16.0,65}{49,6}.100\%=20,97\%\)
Ta có:
\(2H_2SO_4+2e\rightarrow SO_4^{2-}+SO_2\uparrow+2H_2O\)
...............................0,4 <---- 0,4
\(\Rightarrow n_{SO_4^{2-}}\text{tạo muối với cation kim loại}=0,4\) mol
\(\Rightarrow m_{\text{muối}}=m_{\text{kim loại}}+m_{SO_4^{2-}}\text{tạo muối với cation kim loại}\)
\(=56.0,7+96.0,4=77,6\) gam

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)

$n_{SO_2}=\dfrac{2,24}{22,4}=0,1(mol)$
Quy hỗn hợp về $Fe:x(mol),O:y(mol)$
$\to 56x+16y=30,4(1)$
Bảo toàn e: $3n_{Fe}=2n_O+2n_{SO_2}$
$\to 3x=2y+0,2(2)$
Từ $(1)(2)\to x=0,4(mol);y=0,5(mol)$
Bảo toàn Fe: $n_{Fe_2(SO_4)_3}=0,5x=0,2(mol)$
$\to m_X=0,2.400=80(g)$
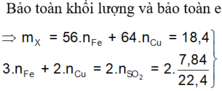
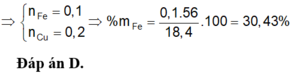
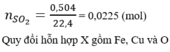
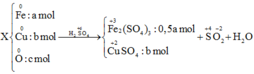
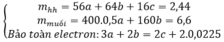
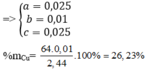
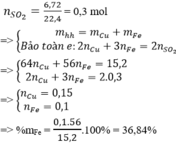


Đối vs bài này ta quy đổi hỗn hợp X thành 2 phần là Fe và O
nên m(hỗn hợp) =mFe+mO=49,6g. (1)
Btoàn e ta có:
Fe--> Fe(+3) +3e; O2 +4e---> 2O(-2) ;
S(+6)---> S(+4) +2e;
---> 3*nFe+ 2*nSO2=2*nO =2*nO - 0,8; (2)
từ (1) và (2) ta có mO=19.36(g);mFe= 30,24(g);
a) %O=19,36/49,6 =39,03%;
b) bảo toàn nguyên tố Fe ta có:
nFe2(SO4)3 =2nFe=2*30,24/46=1,08 mol;
khối lượng muối trong ddY là 1,08*(56*2+96*3)=432 g.