

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Gọi kim loại kiềm và kim loại kiềm thổ là A, B
\(\left\{{}\begin{matrix}n_A=a\left(mol\right)\\n_B=b\left(mol\right)\end{matrix}\right.\)
=> a.MA + b.MB = 42,6 (*)
Và \(\dfrac{a}{b}=\dfrac{5}{4}\Rightarrow b=0,8a\)
\(n_{H_2}=\dfrac{17,472}{22,4}=0,78\left(mol\right)\)
\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
Do \(n_{HCl}< 2.n_{H_2}\) => HCl pư hết, có phản ứng của kim loại với H2O
PTHH: 2A + 2HCl --> 2ACl + H2 (1)
B + 2HCl --> BCl2 + H2 (2)
2A + 2H2O --> 2AOH + H2 (3)
B + 2H2O --> B(OH)2 + H2 (4)
(1)(3) => \(n_{H_2}=\dfrac{1}{2}.n_A=0,5a\left(mol\right)\)
(2)(4) => \(n_{H_2}=n_B=0,8a\left(mol\right)\)
=> \(0,5a+0,8a=0,78\Rightarrow a=0,6\left(mol\right)\Rightarrow b=0,48\left(mol\right)\)
(*) => 0,6.MA + 0,48.MB = 42,6
=> MA + 0,8.MB = 71
=> Chọn \(\left\{{}\begin{matrix}M_A=39\left(K\right)\\M_B=40\left(Ca\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}n_{Ca}=0,48\left(mol\right)\\n_K=0,6\left(mol\right)\end{matrix}\right.\)
Y chứa \(\left\{{}\begin{matrix}n_{Ca^{2+}}=0,48\left(mol\right)\\n_{K^+}=0,6\left(mol\right)\\n_{Cl^-}=0,5\left(mol\right)\\n_{OH^-}=x\left(mol\right)\end{matrix}\right.\)
Bảo toàn điện tích: 2.0,48 + 0,6 = 0,5 + x
=> x = 1,06
- TH1:
2OH- + CO2 --> CO32- + H2O
0,48<----0,48
CO32- + Ca2+ --> CaCO3
0,48<--0,48
=> nCO2 = 0,48 (mol)
- TH2:
2OH- + CO2 --> CO32- + H2O
1,06-->0,53---->0,53
CO32- + Ca2+ --> CaCO3
0,48<--0,48
CO32- + CO2 + H2O --> 2HCO3-
0,05-->0,05
=> nCO2 = 0,58 (mol)
=> \(0,48\le n_{CO_2}\le0,58\)
=> \(10,752\le V_{CO_2}\le12,992\)
nếu k dùng pt ion bn có thể lm nnay
Ca + 2HCl --> CaCl2 + H2
a-->2a-------->a
2K + 2HCl --> 2KCl + H2
b----->b-------->b
2K + 2H2O --> 2KOH + H2
c---------------->c
Ca + 2H2O --> Ca(OH)2 + H2
d------------------->d
=> \(\left\{{}\begin{matrix}a+d=0,48\\b+c=0,6\\2a+b=0,5\end{matrix}\right.\) => 2d + c = 1,06
TH1:
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
d------->d----------->d
2KOH + CO2 --> K2CO3 + H2O
2a---->a-------->a
K2CO3 + CaCl2 --> CaCO3 + 2KCl
a<-------a----------->a
Điều kiện: \(2a\le c\)
<=> \(2a-c\le0\)
<=> \(2\left(0,48-d\right)-\left(1,06-2d\right)\le0\)
<=> \(0\le0,1\) (luôn đúng)
Vậy nkt max = a + d = 0,48 <=> nCO2 min = a + d = 0,48 (mol)
<=> VCO2 min = 10,752(l) (1)
TH2:
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
d------->d----------->d
2KOH + CO2 --> K2CO3 + H2O
c---->0,5c------>0,5c
K2CO3 + CaCl2 --> CaCO3 + 2KCl
a<-------a----------->a
K2CO3 + CO2 + H2O --> 2KHCO3
(0,5c-a)->(0,5c-a)
Điều kiện: \(0,5c\ge a\) (cmt)
Vậy nkt max = a + d = 0,48 <=> nCO2 max = c+d-a = 0,58 (mol)
<=> VCO2 max = 12,992(l) (2)
(1)(2) => ...

A, B lần lượt là kim loại kiềm, kiềm thổ
2A(a)+2HCl→2ACl+H2(0,5a)2A(a)+2HCl→2ACl+H2(0,5a)(1)(1)
B(b)+2HCl→BCl2+H2(b)B(b)+2HCl→BCl2+H2(b)(2)(2)
nHCl=0,5(mol)nHCl=0,5(mol)
nH2=0,78(mol)nH2=0,78(mol)
Gỉa sử lượng HCl tham gia phản nứng hết
=> nH2 = 1/2nHCl = 0,25 (mol) < 0,78 (mol)
=> A, B còn dư tác dụng với nước có trong dung dịch HCl
2A(1,25x−a)+2H2O→2AOH+H2(0,625x−0,5a)2A(1,25x−a)+2H2O→2AOH+H2(0,625x−0,5a)(3)(3)
B(x−b)+2H2O→B(OH)2+H2(x−b)B(x−b)+2H2O→B(OH)2+H2(x−b)(4)(4)
Ta có: nA:nB=5:4nA:nB=5:4
Gọi x là số mol của B => nA = 1,25x (mol)
⇒1,25xA+xB=42,6(I)⇒1,25xA+xB=42,6(I)
Gọi a, b lần lượt là số mol của A, B ở pt (1) và (2)
Ta có: ∑nH2=0,78=0,5a+b+0,625x+x∑nH2=0,78=0,5a+b+0,625x+x
⇔x=0,48(mol)⇔x=0,48(mol)
Thay vào (I) ⇔0,6A+0,48B=42,6⇔0,6A+0,48B=42,6
- Vói A = 7 (Li) => B = 80 (loại)
- Với A = 23 (Na) => B = 60 (loại)
- Với A = 39 (K) => B = 40 (Ca) thoã mãn
- A = 85 (Rb) = > B = -17,5 (loại)
- A = 133 (Cs) => B = -77,5 (loại)
- A = 223 (Fr) = > B = -290 (loại)
Vậy A: K,
B: Ca

1.
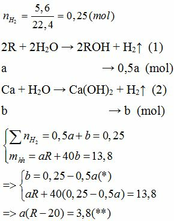
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
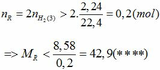
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
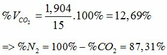
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
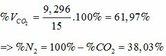

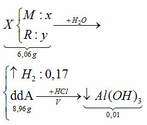
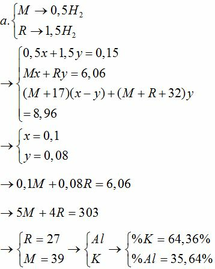
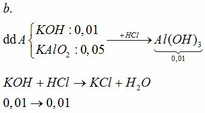
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)