Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Bảo toàn khối lượng: mdung dịch tăng = mMg – mX ⇒ mX = 3,6 – 3,04 = 0,56(g).
⇒ MX = 0,56 ÷ 0,02 = 28 (N2) || Chú ý: "hòa tan hoàn toàn" ⇒ Mg hết.
► Bảo toàn electron: 2nMg = 10nN2 + 8nNH4NO3 ⇒ nNH4NO3 = 0,0125 mol.
Bảo toàn nguyên tố Nitơ: ∑nNO3–/Y = 0,4 – 0,02 × 2 – 0,0125 = 0,3475 mol.
||⇒ Bảo toàn nguyên tố Natri: nNaOH = nNaNO3 = 0,3475 mol ⇒ V = 173,75 ml

Chọn đáp án D
Ta có mKhí = mMg – mdd tăng = 0,56 gam
⇒ MKhí = 0,56 ÷ 0,02 = 28 ⇒ X là khí N2.
Bảo toàn e có nNH4NO3 = (2nMg – 10nN2) ÷ 8 = 0,0125
+ Nhận thấy cuối cùng Na sẽ đi về muối NaNO3 ⇒ Tìm ∑nNO3 có trong dung dịch Y.
Bảo toàn nito ta có nNO3/Y = nHNO3 – 2nN2 – nNH4 = 0,3475 mol.
⇒ nNaOH = 0,3475 mol ⇒ VNaOH = 0,17375 lít = 175,75 ml ⇒ Chọn D

Xét phản ứng Mg tác dụng với dd HNO3, nhận thấy mY tăng=mMg - mX
suy ra mX=3,6-3,04=0,56(gam)
lại có nX=0,448/22,4=0,02(mol) \(\Rightarrow\) MX=0,56/0,02=28
\(\Rightarrow\) X là khí N2
Dễ dàng tìm được dung dịch Y chứa Mg(NO3)2 ; NH4NO3 ; HNO3 dư
Bạn dùng bảo toàn e để tìm số mol NH4NO3
dùng bảo toàn nguyên tố N để tìm HNO3 dư
\(n_{NaOH}=n_{NH_4NO_3}+2n_{Mg\left(NO_3\right)2}+n_{HNO_3dư}\)

Đáp án D
Dung dịch X + vừa đủ 0,25 mol NaOH sinh ra 0,12 mol Mg(OH)2.
+ Nhận thấy để tạo 0,12 mol Mg(OH)2 cần dùng 0,24 mol NaOH < 0,25 mol NaOH cần dùng vừa đủ.
Mà đề nói hỗn hợp M tác dụng vừa đủ với axit HNO3 ⇒ HNO3 không thể dư được.
⇒ Chỉ có 1 cách giải thích thỏa đáng đó là nNH4NO3 = 0,25 – 0,24 = 0,01 mol.
Vậy ta có sơ đồ:
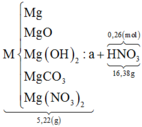
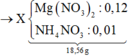
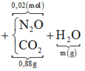
Vì 2 khí có cùng phân tử khối là 44 ⇒ mKhí = 0,02×44 = 0,88 gam.
mMuối = 0,12×148 + 0,01×80 = 18,56 gam.
Vậy bảo toàn khối lượng ta ⇒ mH2O = m = 2,16 gam ⇒ nH2O = 0,12 mol.
ĐẶt nMg(OH)2 = a và bảo toàn hiđro cả quá trình ta có:
2a + 0,26 = 0,01×4 + 0,12×2 ⇔ a = 0,01 mol.
⇒ mMg(OH)2 = 0,01×58 = 0,58 gam.
⇒ %mMg(OH)2 = 0 , 58 × 100 5 , 22 ≈ 11,11%

Đáp án A
Số mol N2O = 1,008/22,4 = 0,045 mol;
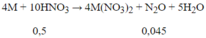
Số mol HNO3 phản ứng = 0,045.10 = 0,45 mol < 0,5 suy ra có tạo sản phẩm khử khác là NH4NO3
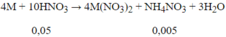
Vậy m = 8,9 + 62.( 8.0,045+8.0,005)+ 80.0.005=34,1g

Đáp án B
![]()
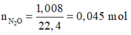
2NO−3 + 10H+ + 8e → N2O↑ + 5H2O
→ n N O 3 - ( m u ố i )
![]()
Ta thấy:
2 n N 2 O + n N O 3 - ( m u ố i ) = 0,045.2 + 0,36 = 0,45 mol < n H N O 3 =>Có muối NH4NO3.
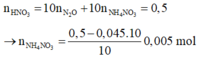
n N O 3 - ( m u ố i ) =
![]()
= 0,4 mol
![]()
![]()

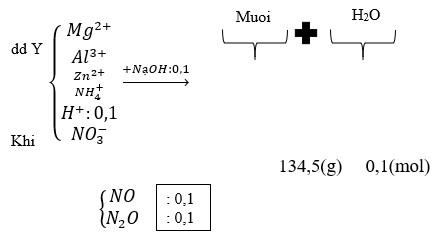



Đáp án D
Bảo toàn khối lượng: mdung dịch tăng = mMg – mX ⇒ mX = 3,6 – 3,04 = 0,56(g).
⇒ MX = 0,56 : 0,02 = 28 (N2)
Chú ý: "hòa tan hoàn toàn" ⇒ Mg hết.
Bảo toàn electron: 2nMg = 10nN2 + 8nNH4NO3 ⇒ nNH4NO3 = 0,0125 mol.
Bảo toàn nguyên tố Nitơ: ∑nNO3–/Y = 0,4 – 0,02 × 2 – 0,0125 = 0,3475 mol.
⇒ Bảo toàn nguyên tố Natri: nNaOH = nNaNO3 = 0,3475 mol ⇒ V = 173,75 ml