Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Mg + 2HCl → MgCl2 + H2 (1)
Al2O3 + 6HCl → 2AlCl3 + 3H2O (2)
nH2 = 2,8/22,4 = 0,125 mol
Theo tỉ lệ phản ứng (1) => nMg = nH2 = 0,125 mol
<=> mMg = 0,125 .24 = 3 gam và mAl2O3 = 8,1 - 3 =5,1 gam
%mMg = \(\dfrac{3}{8,1}\).100% = 37,03% => %mAl2O3 = 100 - 37,03 = 62,97%
b) nAl2O3 = \(\dfrac{5,1}{102}\)= 0,05 mol
=> nHCl pư = 2nMg + 6nAl2O3 = 0,55 mol
mHCl = 0,55.36,5 = 20,075 gam
=> mdung dịch HCl 18% = \(\dfrac{20,075}{18\%}\)= 111,53 gam

Gọi x,y,z lần lượt là số mol của Al,Mg,Zn
PT:
2Al + 6HCl--->2AlCl3 + 3H2
x-------3x----------------------1,5x mol
Mg + 2HCl--->MgCl2 + H2
y-----2y----------------------y mol
Zn + 2HCl--->ZnCl2 + H2
z----2z--------------------z mol
b.
Số mol H2: nH2=16,352/22,4=0,73 mol
1,5x+y+z=0,73
27x = 24y =>x=8y/9
=>7y/3 +z =0,73 (*)
27x + 24y + 65z=19,6
27x = 24y
=> 48y + 65z =19,6 (**)
Từ (*),(**)
=>y=0,27 => mMg =6,48 g
z=0,1=>mZn = 6,5 g
x=0,24=>mAl =6,48g
c.
nHCl =2nH2
=>nHCl =2.0,73=1,46 mol
=>V dd=1,46/2=0,73(l)

a/ nHCl = nH2SO4 = 0,2 x 0,3 = 0,06 mol
nH2 = 1,8816 : 22,4 = 0,082 mol
Ta có: nH (axit) = 0,06 + 0,06 x 2 = 0,18 mol
nH(H2) = 0,084 x 2 = 0,168 mol < 0,18 => axit còn dư
Vậy hỗn hợp kim loại tan hết
b/ Đặt CT tương đương 2 axit là HX
Gọi x, y, z lần lượt là sô mol của Al, Mg, Zn trong hõn hợp
PTHH 2Al + 6HX ===> 2AlX3 + 3H2
Zn + 2HX ===> ZnX2 + H2
Mg + 2HX ===> MgX2 + H2
Sơ đô: 2Al=>3H2 ; Mg => H2 ; Zn=>H2
x 1,5x y y z z (mol)
Theo đề bài ta có hệ pt\(\begin{cases}27x+24y+65z=2,661\\1,5+y+z=0,084\\27x-24y=0\end{cases}\)
=> x = 0,024(mol)
y =0,027(mol)
z=0,021(mol)
=> mZn = 0,021 x 65 = 1,365 gam
=>%mZn = 1,365 / 2,661 = 51,3%

a) $Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
Theo PTHH : $n_{Zn} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$m_{Zn} = 0,2.65 = 13(gam)$
$m_{ZnO} = 21,1 - 13 = 8,1(gam)$
c) $n_{ZnO} = 0,1(mol)$
Theo PTHH : $n_{HCl} = 2n_{Zn} + 2n_{ZnO} = 0,6(mol)$
$m_{dd\ HCl} = \dfrac{0,6.36,5}{16,6\%} = 132(gam)$
d) $m_{dd\ sau\ pư} = 21,1 + 132 - 0,2.2 = 152,7(gam)$
$n_{ZnCl_2} = n_{Zn} + n_{ZnO} = 0,3(mol)$
$C\%_{ZnCl_2} = \dfrac{0,3.136}{152,7}.100\% = 26,72\%$

PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a, Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
⇒ 24x + 27y = 12,6 (1)
Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}y\left(mol\right)\)
\(\Rightarrow x+\dfrac{3}{2}y=0,6\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MG}=\dfrac{0,3.24}{12,6}.100\%\approx57,1\%\\\%m_{Al}\approx42,9\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{H_2SO_4}=n_{H_2}=0,6\left(mol\right)\\n_{MgSO_4}=n_{Mg}=0,3\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{H_2SO_4}=0,6.98=58,8\left(g\right)\Rightarrow m_{ddH_2SO_4}=\dfrac{58,8}{14,7\%}=400\left(g\right)\)
Ta có: m dd sau pư = 12,6 + 400 - 0,6.2 = 411,4 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{0,3.120}{411,4}.100\%\approx8,75\%\\C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1.342}{411,4}.100\%\approx8,31\%\end{matrix}\right.\)
Bạn tham khảo nhé!

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
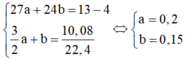
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.
Tham khảo