
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1
1)
$(1) 4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$(2) 2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
$(3) SO_3 + H_2O \to H_2SO_4$
$(4)6FeSO_4 + 3Cl_2 \to 2Fe_2(SO_4)_3 + 2FeCl_3$
$(5) Fe_2(SO_4)_3 + 3BaCl_2 \to 3BaSO_4 + 2FeCl_3$
$(6) FeCl_3 + 3KOH \to Fe(OH)_3 + 3KCl$
$(7) 2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
2)
Trích mẫu thử
Cho dung dịch phenolphtalein vào
- mẫu thử hóa hồng là NaOH
Cho ba mẫu thử còn lai tác dụng lần lượt với nhau
- mẫu thử tạo kết tủa trắng là $H_2SO_4,Ba(NO_3)_2$
$Ba(NO_3)_2 + H_2SO_4 \to BaSO_4 + 2HNO_3$
- mẫu thử không hiện tượng là HCl
Cô cạn hai mẫu thử còn :
- mẫu thử thu được chất rắn khan là $Ba(NO_3)_2$
- mẫu thử không thu được chất rắn là $H_2SO_4$




a) \(n_{Al}=\dfrac{2,43}{27}=0,09;n_{HNO_3}=0,21.2=0,42\)
Al + 4HNO3 → NO + 2H2O + Al(NO3)3
0,09__0,42
Lập tỉ lệ : \(\dfrac{0,09}{1}< \dfrac{0,42}{4}\) => HNO3 dư
Dung dịch X : Al(NO3)3 : 0,09 (mol)
HNO3 dư : (0,42-0,09.4)=0,06 (mol)
b) M + HCl ------> MCl + \(\dfrac{1}{2}\)H2
\(n_M=2n_{H_2}=2.\dfrac{4,2}{22,4}=0,375\left(mol\right)\)
=> \(M_M=\dfrac{8,625}{0,375}=23\left(Na\right)\)


\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3mol\Rightarrow m_C=3,6g\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4mol\Rightarrow n_H=0,4\cdot2=0,8\Rightarrow m_H=0,8g\)
Nhận thấy: \(m_C+m_H=4,4=m_A\)
\(\Rightarrow A\) chỉ chứa hai nguyên tố C và H.
Gọi CTHH là \(C_xH_y\).
\(\Rightarrow x:y=n_C:n_H=0,3:0,8=3:8\)
\(\Rightarrow C_3H_8\)
Gọi CTĐGN là \(\left(C_3H_8\right)_n\)
Mà \(M=44\)g/mol\(\Rightarrow44n=44\Rightarrow n=1\)
Vậy CTPT là \(C_3H_8\)
A không làm mất màu dung dịch brom.





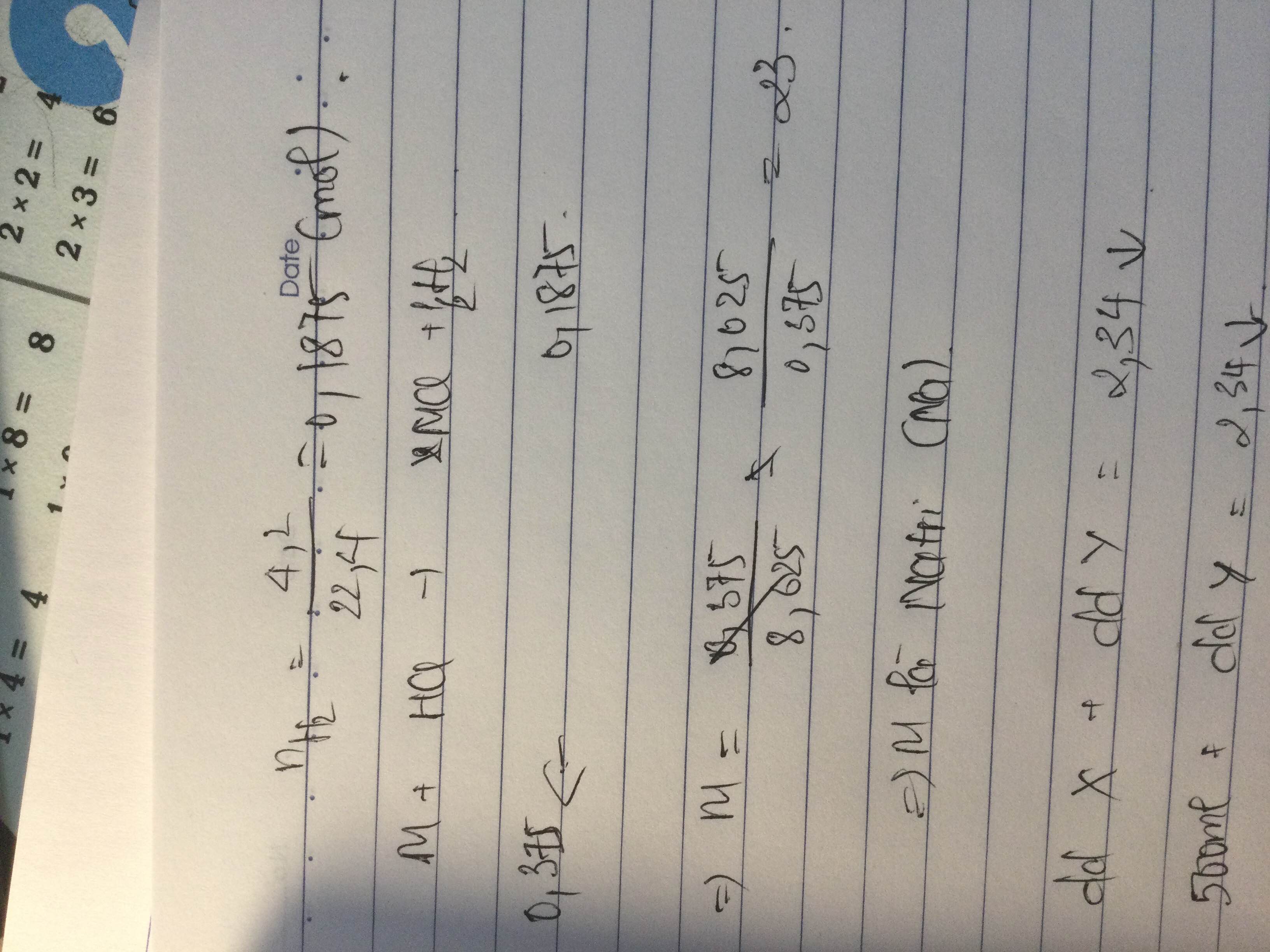
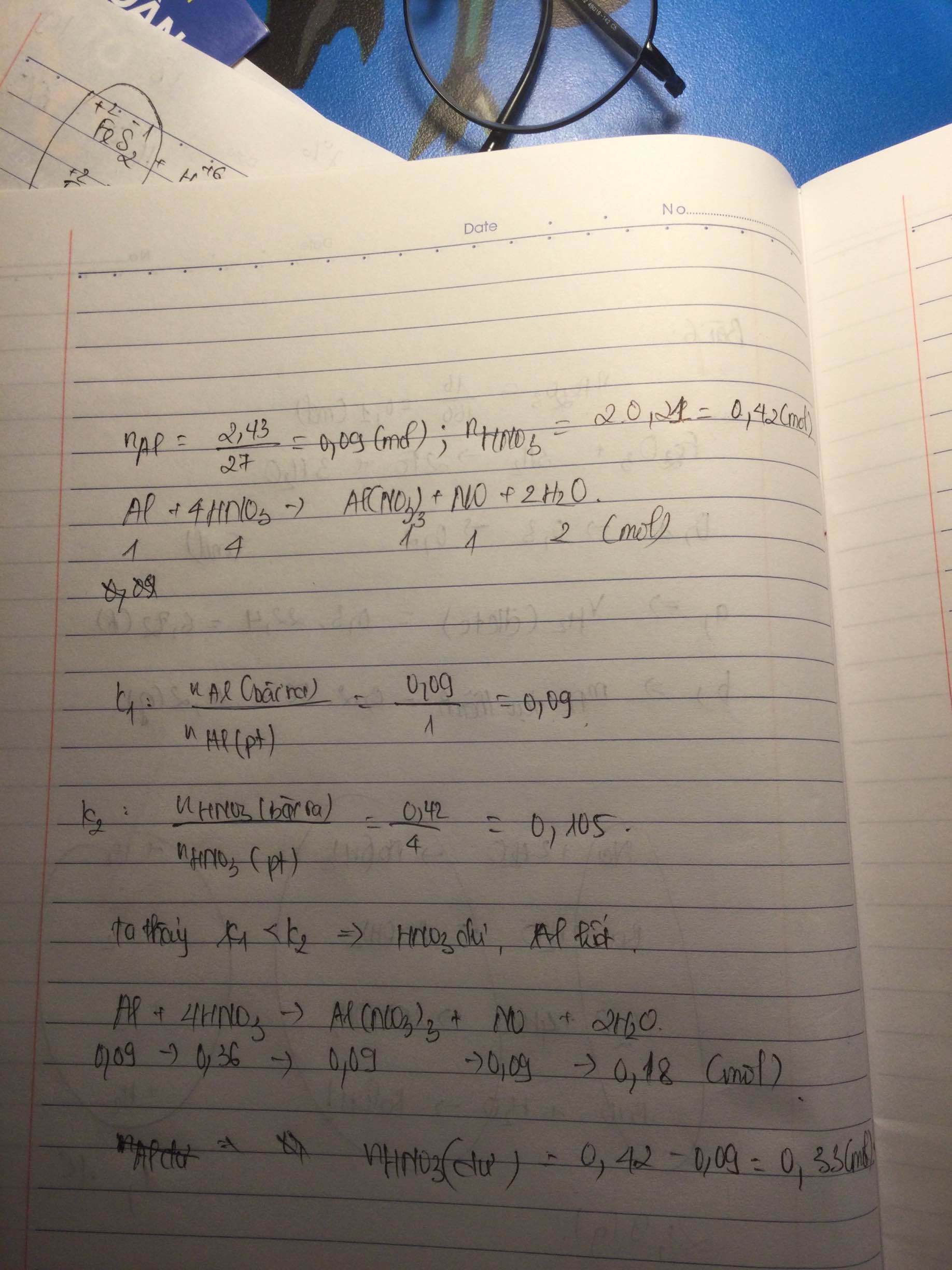



Bài 3 :
\(n_{CaCO3}=\dfrac{10}{100}=0,1\left(mol\right)\)
Pt : \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,1 0,2 0,1 0,1
a) \(n_{CO2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,1.24,79=2,479\left(l\right)\)
b) \(n_{HCl}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(m_{ddHCl}=\dfrac{7,3.100}{7,3}=100\left(g\right)\)
c) \(n_{CaCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{CaCl2}=0,1.111=11,1\left(g\right)\)
\(m_{ddspu}=10+100-\left(0,1.44\right)=105,6\left(g\right)\)
\(C_{CaCl2}=\dfrac{11,1.100}{105,6}=10,51\)0/0
Chúc bạn học tốt