Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phần tính toán :
Theo phương trình hoá học :
124 gam CuCO 3 sau khi bị phân huỷ sinh ra 80 gam CuO.
Vậy 12,4 gam CuCO 3 sau khi bị phân huỷ sinh ra :
m CuO = 80x12,4/124 = 8g
Thí nghiệm được tiến hành trong các ống nghiệm A, B, D là đúng.

Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO ---> 2Fe3O4 + CO2 (1)
Fe3O4 + CO ---->3FeO + CO2 (2)
FeO + CO ---> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành.
mol.
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 - x) = 0,5 * 20,4 * 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA +
m = 64 + 0,4* 44 - 0,4 * 28 = 70,4 gam.

Hướng dẫn :
TN1 cho biết chất đem làm thí nghiệm là muối cacbonat hoặc hiđrocacbonat ( K 2 CO 3 , CaCO 3 , NaHCO 3 , Na 2 CO 3 ).
K 2 CO 3 + 2HCl → 2KCl + H 2 O + CO 2
CaCO 3 + 2HCl → CaCl 2 + H 2 O + CO 2
NaHCO 3 + HCl → NaCl + H 2 O + CO 2
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
TN2 cho biết muối đem làm thí nghiệm là CaCO 3 hoặc NaHCO 3 , là những muối bị phân huỷ ở nhiệt độ cao.
CaCO 3 → CaO + CO 2
2 NaHCO 3 → Na 2 CO 3 + CO 2 + H 2 O
TN3 cho biết sản phẩm thu được ở thí nghiêm 2 phải là muối cacbonat, không thể là canxi oxit CaO.
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
Kết luận : Bạn em đã lấy muối NaHCO 3 làm thí nghiệm.
Viết các phương trình hoá học của phản ứng xảy ra trong ba thí nghiệm trên.

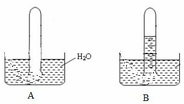
a)- Khí C2H4 không tan trong nước => có thể thu được hoàn toàn khí X bằng cách đẩy nước => hình vẽ A để thu khí C2H4.
- SO2 là khí ít tan trong nước => một phần hòa tan trong nước tạo thành dd axit, phần còn lại không tan ta sẽ thu được khí => hình vẽ B thu khí SO2
SO2 + H2O ⟷ H2SO3
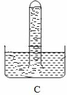
- HCl là khí tan nhiều trong nước => hình vẽ C ứng với thu khí HCl
b)+ Thay nước cất bằng dd nước Br2 thì mực nước trong chậu A và B sẽ dâng cao hết lên đáy ỗng nghiệm, do C2H4 và SO2 cùng có phản ứng với dd nước Br2
C2H4 + Br2 → C2H4Br2
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
+ Thay nước cất bằng dd NaOH thì mực nước trong chậu A không thay đổi do C2H4 không có phản ứng với dd NaOH, còn mực nước trong chậu B dâng lên đáy ống nghiệm do SO2 phản ứng với dd NaOH
SO2 + 2NaOH → Na2SO3 + H2Ó
SO2 + NaOH → NaHSO3

a. Các kim loại và gốc không được ở cạnh nhau:
\(Ba\) và sunfat,\(Ba\) và cacbonat,\(Mg\) và cacbonat,\(Pb\) và clorua,\(Pb\) và sunfat,\(Pb\) và cabonat
Vậy mỗi ống chứa các dd; \(K_2CO_3,Pb\left(NO_3\right)_2,MgSO_4,BaCl_2\)
b.
Nhỏ dd \(HCl\) vào các ống (thí nghiệm thực hiện ở nhiệt độ thấp)
- \(K_2CO_3 \) có khí không màu
- \(Pb\left(NO_3\right)_2\) có kết tủa trắng
\(K_2CO3+2HCl->2KCl+CO_2+H_2O\)
\(Pb\left(NO_3\right)_2+2HCl->PbCl_2+2HNO_3\)
Nhỏ \(NaOH\) vào 2 dung dịch còn lại
- \(MgSO_4\) kết tủa trắng
- Còn lại là \(BaCl_2\)
\(MgSO_4+2NaOH->Mg\left(OH\right)_2+Na_2SO_4\)
Tham khảo nhé !

\(n_{CO}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\)
\(m_B=20.4\cdot2\cdot0.5=20.4\left(g\right)\)
\(\Leftrightarrow28a+44b=20.4\)
\(KĐ:a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m=0.4\cdot44+64-0.4\cdot28=70.4\left(g\right)\)
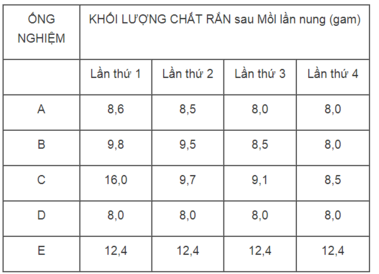
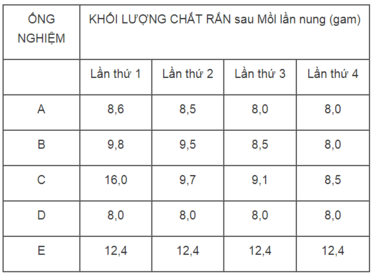
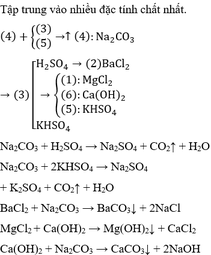

1. Ống nghiệm E (khối lượng CuCO 3 không thay đổi).
2. Ống nghiệm C, vì khác với các kết quả của những ống nghiệm A, B, D.
3. Sau lần nụng thứ 3 thì toàn lượng CuCO 3 đã bị phân huỷ hết thành CuO.
4. Ống nghiệm D.