Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,3\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,3\cdot36,5=10,95\left(g\right)\\m_{Fe}=0,15\cdot56=8,4\left(g\right)\\m_{FeCl_2}=0,15\cdot127=19,05\left(g\right)\end{matrix}\right.\)
PTHH: Fe+2HCl→FeCl2+H2↑Fe+2HCl→FeCl2+H2↑
Ta có: nH2=3,3622,4=0,15(mol)nH2=3,3622,4=0,15(mol)
⇒{nHCl=0,3(mol)nFeCl2=nFe=0,15(mol)⇒{nHCl=0,3(mol)nFeCl2=nFe=0,15(mol) ⇒⎧⎪⎨⎪⎩mHCl=0,3⋅36,5=10,95(g)mFe=0,15⋅56=8,4(g)mFeCl2=0,15⋅127=19,05(g)⇒{mHCl=0,3⋅36,5=10,95(g)mFe=0,15⋅56=8,4(g)mFeCl2=0,15⋅127=19,05(g)

\(n_{Fe}=\dfrac{m}{M}=\dfrac{28}{56}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
ti le 1 : 2 : 1 : 1
n(mol) 0,5-->1--------->0,5------>0,5
\(m_{FeCl_2}=n\cdot M=0,5\cdot\left(56+35,5\cdot2\right)=63,5\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,5\cdot22,4=11,2\left(l\right)\)

\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\\ n_{H_2}=n_{Fe}=0,25\left(mol\right)\\ V_{H_2}=0,25.22,4=5,6\left(l\right)\\ n_{HCl}=2n_{Fe}=0,5\left(mol\right)\\ m_{HCl}=0,5.36,5=18,25\left(g\right)\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ b,n_{HCl}=2n_{H_2}=0,3(mol);n_{FeCl_2}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{HCl}=0,3.36,5=10,95(g)\\ m_{FeCl_2}=0,15.127=19,05(g)\)

\(n_{Fe}=\dfrac{28}{56}=0,5mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5 1 0,5
\(V_{H_2}=0,5\cdot22,4=11,2l\)
\(m_{HCl}=1\cdot36,5=36,5g\)

Gỉai:
a) nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{11,2}{56}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl -> FeCl2 + H2
b) Theo PTHH và đề bài , ta có:
\(n_{H_2}=n_{Fe}=0,2\left(mol\right)\)
Thể tích khí hiđro thu được (đktc):
=> \(V_{H_2\left(đktc\right)}=n_{H_2}.22,4=0,2.22,4=4,48\left(l\right)\)
c) Ta có: nHCl= 2.nFe= 2.0,2=0,4(mol)
Khối lượng HCl cần dùng trong phản ứng:
mHCl=nHCl.MHCl= 0,4.36,5= 14,6(g)
d) Ta có:
\(n_{FeCl_2}=n_{Fe}=0,2\left(mol\right)\)
Khối lượng FeCl2 tạo thành:
\(m_{FeCl_2}=n_{FeCl_2}.M_{FeCl_2}=0,2.127=25,4\left(g\right)\)
a. PTHH: Fe + 2HCl ===> FeCl2 + H2
b. Số mol Fe: nFe = \(\frac{11,2}{56}=0,2\left(mol\right)\)
Theo phương trình, ta có: nH2 = nFe = 0,2 (mol)
=> Thể tích H2 thu được: VH2(đktc) = 0,2 x 22,4 = 4,48 (lít)
c. Theo phương trình, nHCl = 2nFe = 0,4 (mol)
=> Khối lượng HCl cần dùng là: mHCl = 0,4 x 36,5 = 14,6 (gam)
d. Theo phương trình, nFeCl2 = nFe = 0,2 (mol)
=> Khối lượng FeCl2 tạo thành: mFeCl2 = 0,2 x 127 = 25,4 (gam)

Bảo toàn KL: \(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{FeCl_2}=5,6+7,3-0,2=12,7(g)\)

a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<---0,4<------0,2<--0,2
=> mFe = 0,2.56 = 11,2 (g)
b) mFeCl2 = 0,2.127 = 25,4 (g)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\
pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,2 0,2
\(m_{Fe}=0,2.56=11,2g\\
m_{FeCl_2}=127.0,2=25,4g\)

\(a,n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{HCl}=2.n_{Fe}=2.0,1=0,2\left(mol\right)\\ m_{HCl}=0,2.36,5=7,3\left(g\right)\\ b,n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
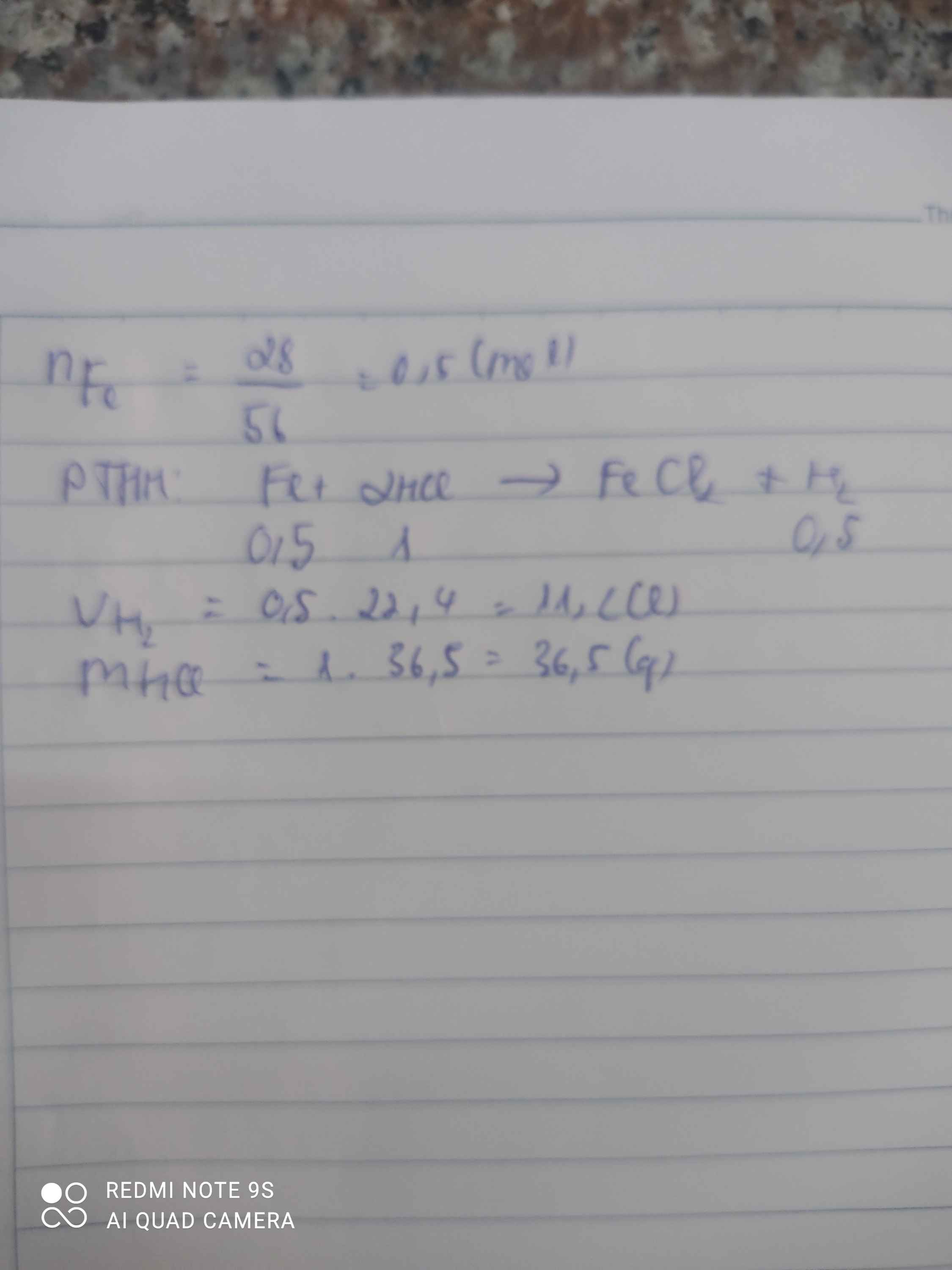
a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<--0,3<-----0,15<--0,15
=> \(m_{Fe}=0,15.56=8,4\left(g\right)\)
=> \(m_{HCl}=0,3.36,5=10,95\left(g\right)\)
b) \(m_{FeCl_2}=0,15.127=19,05\left(g\right)\)