Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Vì là kim loại phản ứng với dung dịch kiềm, giải phóng khí hiđro và nhẹ dẫn điện, dẫn nhiệt tốt
=> kim loại đó là Al

Phát biểu đúng: b). Vậy số phát biểu đúng là 1
Các phát biểu sai là:
a) Metan cháy với oxi tạo hơi nước và khí lưu huỳnh đioxit => Sai vì tạo khí cacbonic ( C O 2 ) chứ không phải là lưu huỳnh đioxit
c) Trong phản ứng hóa học giữa Metan và Clo, chỉ có duy nhất một nguyên tử Hiđro của Metan có thể được thay thế bởi nguyên tử Clo => Sai.
d) Hỗn hợp gồm hai thể tích Metan và một thể tích Oxi là hỗn hợp nổ mạnh => Sai, hỗn hợp nổ gồm một thể tích Metan và hai phần thể tích Oxi
Đáp án: A

(a) Phản ứng nổ của TNT: 2C7H5N3O6 → 3N2 + 5H2O + 7CO + 7C
(b) 100 gam thuốc nổ Hexanit có chứa 60 gam TNT và 40 gam HND.
Số mol của từng chất là:
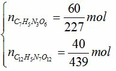
Áp dụng định luật bảo toàn nguyên tố ta có:
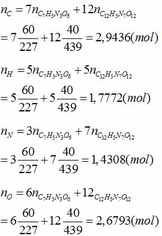
- Phần trăm khối lượng mỗi nguyên tố trong Hexanit:
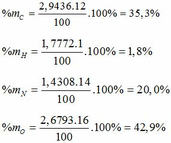
- Sản phẩm nổ của Hexanit là N2, H2O, CO, C
- Áp dụng định luật bảo toàn nguyên tố ta tính được số mol của các chất trong hỗn hợp sau khi nổ:
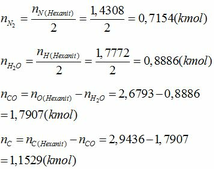
Phần trăm số mol của các chất trong hỗn hợp sau khi nổ:
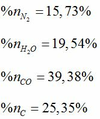

a) MD = R + 32 (g/mol)
ME = R + n (g/mol)
Theo đề bài \(\dfrac{M_D}{M_E}\)= \(\dfrac{R+32}{R+n}\)= \(\dfrac{32}{17}\) => \(\left\{{}\begin{matrix}n=2\\R=32\end{matrix}\right.\) là giá trị thỏa mãn
Vậy R là lưu huỳnh (S)
b) m 100ml dung dịch HCl = 1,2.100 = 120 gam
M2SO3 + 2HCl → 2MCl + SO2↑ + H2O
m dung dịch sau phản ứng = m M2SO3 + m dung dịch HCl - m SO2 = 126,2 gam
=> 12,6 + 120 - 126,2 = mSO2
<=> mSO2 = 6,4 gam , nSO2 = 6,4 : 64 = 0,1 mol
Theo phương trình phản ứng , nM2SO3 = nSO2 = 0,1 mol
=> MM2SO3 = \(\dfrac{12,6}{0,1}\)= 126 (g/mol)
=> MM = (126 - 32 - 16.3) : 2 = 23 g/mol
Vậy M là natri (Na)



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


a) thù hình Ví dụ: O2 và O3. S2, S8 và Sn.
b) nhiệt độ nóng chảy cao. Nhà bác học Edison phải mất 10.000 thí nghiệm mới tìm ra được vật liệu W sử dụng trong dây tóc bóng đèn.
c) anot. Thu được Na ở catot (cực –) và Cl2 ở anot (cực +)
d) HF Các vật liệu thủy tinh có cấu tạo bởi SiO2, và: SiO2 + 4HF → SiF4 + 2H2O

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
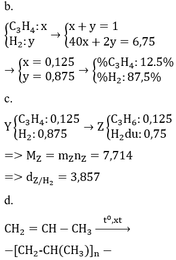


a.
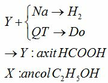
b.Chọn vôi tôi hoặc nếu có kem đánh răng cũng được
2HCOOH + Ca(OH)2 → (HCOO)2Ca + 2H2O
c) HCOOH + Na → HCOONa + ½ H2
C2H5OH + Na → C2H5ONa + ½ H2
n(X, Y) = 2.nH2 → nH2 = 0,15 → V = 3,36 (lít)
a. nguyên tố; hiđrô; oxi; kim loại; oxit bazơ; oxit axit.
d. nguyên tử hiđrô;gốc axit.
c. nguyên tố; hiđrô; oxi; kim loại; oxit bazơ; oxit axit.