Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có nAg = 0,2 mol
Trường hợp 1: Anđehit HCHO
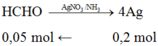
=> mHCHO = 0,05.30 = 1,5g ≠ 2,9g => Loại
Trường hợp 2 : Anđehit không phải HCHO
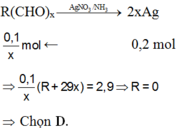

Đáp án D
nAg = 21,6 : 108 = 0,2 (mol)
=> nRCHO = nAg/2 = 0,1 (mol)
=> MRCHO = 4,4 : 0,1 = 44 (g/mol) => CH3CHO

Đáp án D
nAg = 21,6 : 108 = 0,2 (mol)
=> nRCHO = nAg/2 = 0,1 (mol)
=> MRCHO = 4,4 : 0,1 = 44 (g/mol) => CH3CHO

Đáp án D
nAg = 21,6 : 108 = 0,2 (mol)
=> nRCHO = nAg/2 = 0,1 (mol)
=> MRCHO = 4,4 : 0,1 = 44 (g/mol) => CH3CHO

Đáp án A
n a n d e h i t = 0 , 08 ( m o l ) ; n A g = 0 , 2 ( m o l ) ⇒ n A g n a n d e h i t = 2 , 5
Do X và Y đều đơn chức => X hoặc Y là HCHO.
Vì MX > MY =>Y là HCHO
Gọi công thức của X là RCHO(amol) và n H C H O = b ( m o l )
⇒ a + b = 0 , 08 (1)
Lại có: nAg = 2nRCHO + 4nHCHO = 2a + 4b = 0,2(mol) (2)
Từ (1) và (2) => a = 0,06(mol); b = 0,02(mol)
=> nX = 0,06(mol).
Mà mX = 3,36(g) MX = 56 ⇒ X là C2H3CHO

Đáp án D
n H 2 = 0 , 05 ( m o l ) ; n A g = 0 , 08 ( m o l ) T a c ó : n H 2 = 2 n a n d e h i t
=> anđehit no, 2 chức hoặc anđehit đơn chức có 1 liên kết đôi (1).
Lại có: n A g n a n d e h i t < 4
=>trong 2 anđehit có một anđehit phản ứng với AgNO3 theo tỉ lệ 1:2 (2)
Từ (1) và (2) => trong X có một anđehit no, 2 chức (a mol); 1 anđehot không no, đơn chức (b mol)
⇒ a + b = 0 , 025 4 a + 2 b = 0 , 08 ⇒ a = 0 , 015 ( m o l ) b = 0 , 01 ( m o l )
Đến đây ta có thể dựa vào khối lượng của 2 anđehit để tìm được 2 anđehit hoặc ta có thể thử 2 đáp án A và D xem đáp án nào thỏa mãn giá trị tổng khối lượng là 1,64 gam.

\(n_{Ag}=\dfrac{51,84}{108}=0,48\left(mol\right)\)
Xét 2 trường hợp :
TH1 : Andehit là HCHO
\(\Rightarrow n_{HCHO}=\dfrac{3,6}{30}=0,12\left(mol\right)\)
HCHO + 4AgNO3 + 4NH3 + H2O → 4Ag + 4NH4NO3 + CO2
Theo PT : \(n_{Ag}=\dfrac{1}{4}n_{HCHO}=0,12\left(mol\right)=n_{andehit}\)
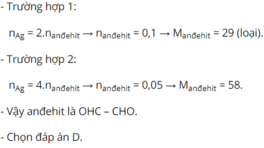
Vì TH1 thỏa mãn nên chắc chắc TH2 loại
Vậy andehit là HCHO
Ta có nAg = 0,2 mol
Trường hợp 1: Anđehit HCHO
Trường hợp 2 : Anđehit không phải HCHO