Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Quy đổi hỗn hợp về Fe (x mol); Cu (y mol) và S (z mol)
Bảo toàn S có
nS = n↓ = 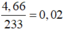 (mol)
(mol)
mX = 2,72 gam → 56x + 64y + 0,02.32 = 2,72 → 56x + 64y = 2,08 (1)
Do Y có thể hòa tan được Cu, bảo toàn electron có:
3.nFe + 2.nCu + 6.nS = 3.0,07 → 3x + 2y = 0,09 (2)
Từ (1) và (2) có: x = 0,02 và y = 0,015.
Dung dịch Y gồm: Fe3+: 0,02 mol; Cu2+: 0,015 mol; SO42- = 0,02 mol; NO3- = (0,5 – 0,07 = 0,43 mol) và có thể có H+
Bảo toàn điện tích → nH+ = 0,38 mol
Cho Cu vào Y có phản ứng:
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
0,1425 ← 0,38 0,43 mol
Cu + 2Fe3+ → Cu2+ + 2Fe2+
0,01 ← 0,02 mol
m = (0,01 + 0,1425).64 = 9,76 gam.

\(n_{Cu} = 0,1\ mol\\ n_{HNO_3} = 0,6\ mol\)
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
0,1........\(\dfrac{4}{15}\)..........................................................(mol)
\(n_{H^+\ dư} = 0,6 - \dfrac{4}{15} = \dfrac{1}{3}(mol)\)
Khi thêm HCl,\(n_{H^+} = \dfrac{1}{3} + 0,2.2 = \dfrac{11}{15}\)
\(3Cu + 8H^+ + 2NO_3^- \to 3Cu^{2+} + 2NO + 4H_2O\)
\(n_{H^+} < 4n_{NO_3^-} = 0,6.4\) nên NO3- dư.
Theo PTHH :
\(n_{Cu} = \dfrac{3}{8}n_{H^+} = \dfrac{3}{8}.\dfrac{11}{15} = 0,275(mol)\\ \Rightarrow m_{Cu} = 0,275.64 = 17,6(gam)\)

\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{HNO_3}=1.0,5=0,5\left(mol\right)\)
PTHH: Fe + 4HNO3 --> Fe(NO3)3 + NO + 2H2O
0,1--->0,4---------->0,1
=> dd sau pư chứa \(\left\{{}\begin{matrix}Fe\left(NO_3\right)_3:0,1\left(mol\right)\\HNO_{3\left(dư\right)}:0,5-0,4=0,1\left(mol\right)\end{matrix}\right.\)
PTHH: 3Cu + 8HNO3 --> 3Cu(NO3)2 + 2NO + 4H2O
0,0375<-0,1
2Fe(NO3)3 + Cu --> 2Fe(NO3)2 + Cu(NO3)2
0,1---->0,05
=> m = (0,0375 + 0,05).64 = 5,6 (g)

\(n_{H^+} = n_{HCl} + n_{HNO_3} = 0,4 + 0,4.1,2 = 0,88\)
\(Gọi\ n_{Fe} = a ;n_O = b ; n_{NO} = c\)
Suy ra :
56a + 16b = 12,48(1)
Bảo toàn electron : 3a = 2b + 3c(2)
\(n_{H^+\ pư} = 2n_O + 4n_{NO} = 2b + 4c(mol)\\ n_{H^+\ dư} = 0,88 - 2b - 4c\)
\(2Fe^{3+} + Cu \to Cu^{2+} + 2Fe^{2+}\\ 3Cu + 8H^+ + 2NO_3^- \to 3Cu^{2+} + 2NO + 4H_2O\)
\(n_{Cu} = 0,12(mol)\)
Theo PTHH :
0,5a + \(\dfrac{3}{8}\)(0,88 - 2b -4c) = 0,12(3)
(1)(2)(3) suy ra a = 0,216 ; b = 0,024 ; c = 0,2
Suy ra V = 0,2.22,4 = 4,48(lít).Đáp án B

Coi hh gồm Fe và O.
Ta có: 56nFe + 16nO = 14,64 (1)
Ta có: \(n_{NO}=\dfrac{1,4874}{24,79}=0,06\left(mol\right)\)
Theo ĐLBT e, có: 3nFe = 2nO + 3nNO ⇒ 3nFe - 2nO = 0,06.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,201\left(mol\right)\\n_O=0,2115\left(mol\right)\end{matrix}\right.\)
⇒ m = mFe = 0,201.56 = 11,256 (g)