Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m b nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.

Khối lượng từng phần là : ![]()
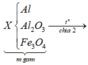
Phản ứng nhiệt nhôm: 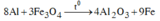
=> Hỗn hợp X gồm Al2O3, Fe, Al dư, Fe3O4 dư
Xét phần hai:
X tác dụng với dung dịch HNO3 cũng chính là hỗn hợp ban đầu Al (a mol) và Fe3O4 (b mol) tác dụng với dung dịch HNO3
![]()
Quy đổi hỗn hợp ban đầu thành Al: a mol; Fe: 3b mol; O:4b mol
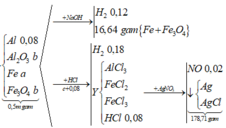
Sơ đồ phản ứng:
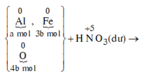
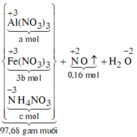
![]()
![]()
![]()
![]()
![]() ]
]
![]()
![]() c = 0,0375 mol
c = 0,0375 mol
-Xét phần một:
Số mol H2 thu được là: ![]()
Sơ đồ phản ứng tạo khí H2 : 
![]()
![]()
![]()
![]()
-Xét phản ứng nhiệt nhôm:
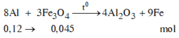
![]()
Đáp án B.

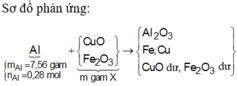
nAl = 0,32
Phần 1: => nAl dư = 0,04 mol => Hỗn hợp có Fe, Cu, Al và Al2O3, nAl2O3 = 0,06 mol
=> nO = 0,18 => nFe + nCu = 0,18
Phần 2: ne nhận = 0,56 mol
=> 3nFe + 2nCu = 0,56 - 0,04.3
=> nFe = 0,08; nCu = 0,1 mol
=> Muối có 0,08 mol Fe(NO3)3, 0,1 mol Cu(NO3)2 và 0,16 mol Al(NO3)3
=> m = 72,24 gam
=> Đáp án B




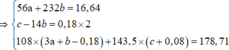
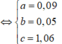

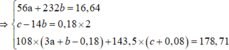
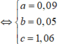

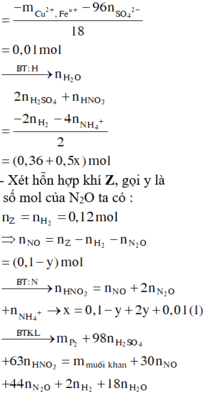


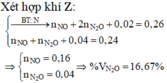

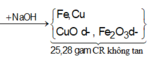
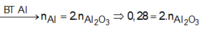

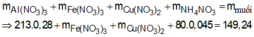
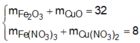

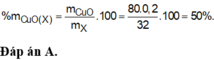
Đáp án C
Đồng nhất số liệu bằng cách nhân đôi giả thiết ở 2 phần
- Giải phần 1: chỉ có Al tạo khí: 2Al + 2NaOH 2NaAlO2 + 3H2 → đọc ra từ 0,12 mol H2 có 0,08 mol Al; mà
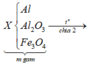
ó Phản ứng nhiệt nhôm:
Giả sử hỗn hợp X có x mol Fe3O4 và y mol CuO ta có: 233x + 80y = 43,84 gam (1)
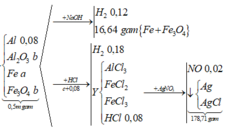
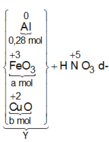
- Giải phần 2: vì dùng dư HNO3 nên hỗn hợp đầu hay Y tác dụng đều cho cùng sản phẩm.
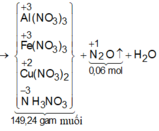
ó Rõ hơn, ta có sơ đồ quá trình: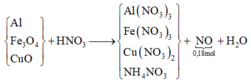
Bảo toàn electron ta có:
Giải hệ các phương trình (1) và (2) ta được: x = 0,12 mol và y = 0,2 mol.
Vậy, m gam X gồm 27,84 gam Fe3O4 và 16,0 gam CuO.