Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) nMg:a(mol) ,nAl:b(mol)
nNO=2,464/22,4=0,11(mol)
hpt: mX=24a+27b=3,42
nNO=23a+b=0,11
→a=0,075(mol),b=0,06(mol)
%mMg=(0,075.24/3,42).100%=52,63%
%mAl=100%−52,63%=47,37%
b)
nHNO3=4nNO=0,44(mol)
mdd HNO3=(0,44.63)/10%=277,2(g)

Ta có: \(n_{NO}+n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\left(1\right)\)
\(30n_{NO}+28n_{N_2}=1,44\left(g\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,02\left(mol\right)\\n_{N_2}=0,03\left(mol\right)\end{matrix}\right.\)
Gọi nNH4NO3 = a (mol)
⇒ nNO3- (trong muối) = 3nNO + 10nN2 + 8nNH4NO3 = 0,36 + 8a (mol)
Ta có: m muối = mKL + mNO3- (trong muối) + mNH4NO3
⇒ 66,88 = 10 + 62.(0,36 + 8a) + 80a
⇒ a = 0,06 (mol)
⇒ nHNO3 = 4nNO + 12nN2 + 10nNH4NO3 = 1,04 (mol)
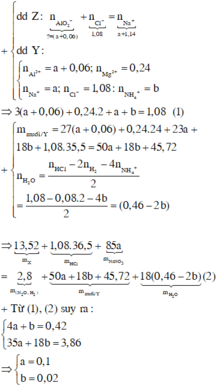
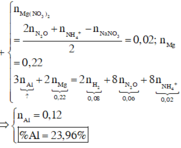
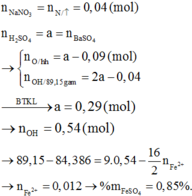





\(n_{Mg}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(24a+27b=15\left(1\right)\)
Bảo toàn e :
\(2a+3b=0.1\cdot\left(2+3+1+8\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=0.4,b=0.2\)
\(\%Mg=64\%,\%Al=36\%\)
Gọi số mol Mg và Al lần lượt là a;b(mol)
$\Rightarrow 24a+27b=15$
Bảo toàn e ta có: $2a+3b=1,4$
Giải hệ ta được $a=0,4;b=0,2$
$\Rightarrow \%m_{Mg}=64\%;\%m_{Al}=36\%$