hòa tan hoàn toàn 1,625 gam kim loại zn vào 3,65g hcl loãng thì thấy có khí h2 thoát ra . a. tính thể tích khí h2 (đktc) thu được sau phản ứng b. chất nào còn dư sau phản ứng và dư bao nhiêu gam c. tính khối lượng muối thu được sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$n_{Fe}=\dfrac{2,24}{56}=0,04(mol)$
$a,PTHH:Fe+2HCl\to FeCl_2+H_2$
$b,$ Theo PT: $n_{H_2}=n_{Fe}=0,04(mol)$
$\Rightarrow V_{H_2}=0,04.22,4=0,896(l)$

\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=2\cdot0,15=0,3\left(mol\right)\)
Vì \(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\) nên sau p/ứ Zn dư
\(\Rightarrow n_{Zn}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\\ \Rightarrow m_{Zn}=0,15\cdot65=9,75\\ \Rightarrow m_{Zn\left(dư\right)}=13-9,75=3,25\left(g\right)\\ c,n_{H_2}=n_{Zn}=0,15\left(mol\right)\\ \Rightarrow V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\)

\(n_{Zn}=\dfrac{16,25}{65}=0,25\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,25\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)
Zn + 2HCl -> ZnCl2 + H2
0.25 0.25
nZn = 0.25 mol
\(V_{H2}=0.25\times22.4=5.6l\)

a. Để tính khối lượng HCl đã dùng, ta cần biết số mol của Al đã phản ứng với HCl. Ta sử dụng phương trình phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Theo đó, 2 mol Al tương ứng với 6 mol HCl. Vậy số mol HCl cần để phản ứng với 2,7 g Al là:
n(HCl) = n(Al) x (6/2) = 2,7/(27x2) x 6 = 0,05 mol
Khối lượng HCl tương ứng là:
m(HCl) = n(HCl) x M(HCl) = 0,05 x 36,5 = 1,825 g
Vậy khối lượng HCl đã dùng là 1,825 g.
b. Theo phương trình phản ứng, 2 mol Al tạo ra 3 mol H2. Vậy số mol H2 tạo ra từ 2,7 g Al là:
n(H2) = n(Al) x (3/2) = 2,7/(27x2) x 3 = 0,025 mol
Theo định luật Avogadro, 1 mol khí ở ĐKTC chiếm thể tích 22,4 L. Vậy thể tích H2 thu được là:
V(H2) = n(H2) x 22,4 = 0,025 x 22,4 = 0,56 L
P.c. CuO + H2 → Cu + H2O
Khối lượng CuO cần để khử hết 0,025 mol H2 là:
n(CuO) = n(H2)/2 = 0,0125 mol
m(CuO) = n(CuO) x M(CuO) = 0,0125 x 79,5 = 0,994 g
Vậy để khử hết H2, ta cần dùng 0,994 g CuO. Nếu dùng toàn bộ lượng H2 bay ra, chất CuO sẽ bị khử hoàn toàn thành Cu và không còn chất nào còn dư.

Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án A
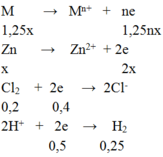
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án B.
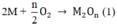
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
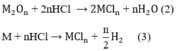
Số mol H2: 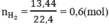
Theo phương trình (1)
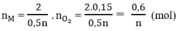
Theo phương trình (3)
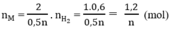
Tổng số mol M là 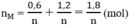
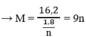
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

\(n_{Zn}=\dfrac{1,625}{65}=0,025mol\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,025 < 0,1 ( mol )
0,025 0,05 0,025 0,025 ( mol )
\(V_{H_2}=0,025.22,4=0,56l\)
Chất dư là HCl
\(m_{HCl\left(dư\right)}=\left(0,1-0,05\right).36,5=1,825g\)
\(m_{ZnCl_2}=0,025.136=3,4g\)
huhu cảm ơn bạn đề dài quá nên đưa lên đây làm giúp