Cho thanh Al vào dung dịch chứa 0,6 mol AGNO3. Sau khi phản ứng đã xảy ra hoàn toàn, lấy thanh Al ra, sấy khô rồi cân lại. Hỏi khối lượng thanh Al tăng hay giảm bao nhiêu gam? Biết răng toàn bộ lượng Ag sinh ra bám hết vào thanh Al.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nAgNO3 = 0,2. 1 = 0,2 (mol)
PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
Theo PTHH: nCu = ½ nAgNO3 = ½. 0,2 = 0,1 (mol)
=> mCu = 0,1.64 = 6,4 (g)
Theo PTHH: nAg = nAgNO3 = 0,2 (mol) => mAg = 0,2.108 = 21,6 (g)
Vì Ag sinh ra đều bám hết vào thanh đồng => khối lượng thanh đồng tăng số gam là :
∆ = mAgsinh ra - mCu pư = 21,6 – 6.4 = 15,2 (g)

Chọn A
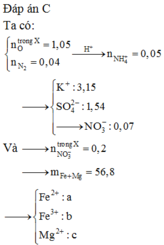
nH+ = 12nN2 + 10nNH4+ + 2nO (oxit) ⇒ nNH4+ = 0,05
Trong dung dịch Y có a mol Mg2+; b mol Fe3+; c mol Fe2+
⇒ nKOH = 2a + 3b + 2c + nNH4+ = 3,15 ⇒ 2a + 3b + 2c = 3,1 (1)
Sau khi tác dụng với KOH thì phần dung dịch chứa 3,15 mol K+; 1,54 mol SO42- và nNO3- = 0,07
Bảo toàn N ⇒ nNO3- ban đầu = 2nN2 + nNH4+ + nNO3- (trong Y) = 0,2
⇒ mX = 24a + 56(b + c) + 62.0,2 + 1,05.16 = 86 (2)
Bảo toàn ne ⇒ 3nAl phản ứng = 3nFe3+ + 2nFe2+ ⇒ nAl phản ứng = b + 2c/3
⇒ mtăng = 56(b + c) – 27(b + 2c/3) = 28 (3)
(1), (2), (3) ⇒ a = 0,15; b = 0,9; c = 0,05
Oxit thu được gồm MgO (0,15 mol) và Fe2O3 (0,95/2 = 0,475) ⇒ m = 0,15.40 + 0,475.160 = 82

Đáp án C
nHNO3 = 0,68; nNO = 0,12
nHNO3 = 4nNO+ 10nNH4NO3=> nNH4NO3 = 0,02 => ne = 3nNO + 8nNH4NO3 = 0,52
mmuối = mkim loại + 62ne + mNH4NO3=> 2,5m + 8,49 = m + 62.0,52 + 80.0,02 => m = 16,9
Bảo toàn ne=>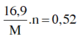 =>
=> 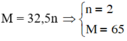

Đáp án C
F e + A g N O 3 0 , 03 m o l C u N O 3 2 0 , 04 m o l
Khối lượng Fe tăng m gam.
Fe + 3Ag+ → Fe2+ + 2Ag↓
Fe + Cu2+ → Fe2+ + Cu↓
Ta có:
mFe tăng = mAg + mCu - mFe phản ứng = 0,03 × 108 + 0,04 × 64 - (0,015 + 0,04) × 56 = 2,72 gam
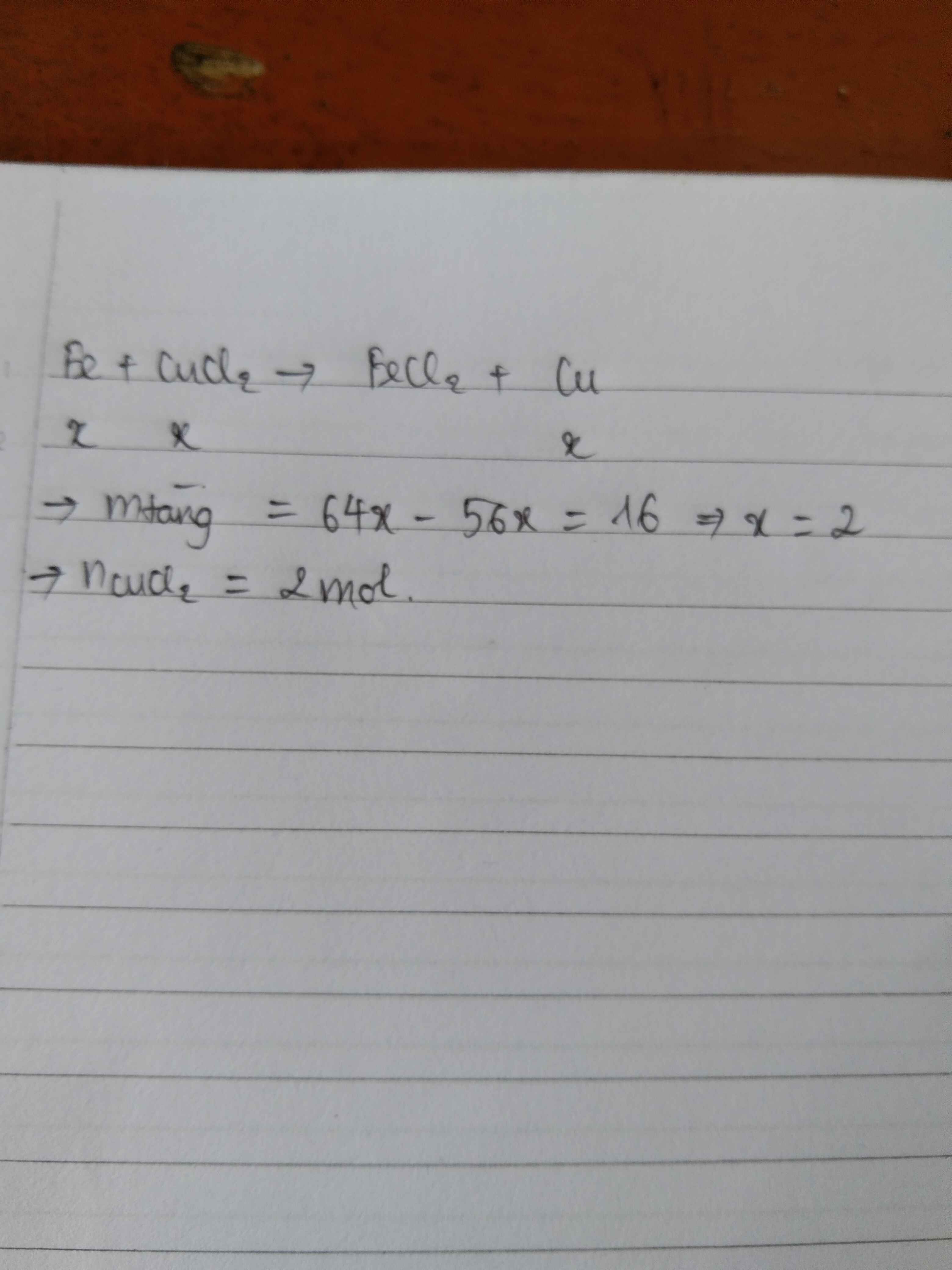
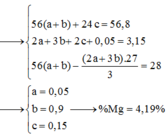

Đáp án:
Tăng 27,6g
Giải thích các bước giải:
2Al+3CuCl2→2AlCl3+3CunAl phản ứng =0,6×23=0,4molnCu=nCuCl2=0,6molm thanh Al tăng =mCu−mAl phản ứng =0,6×64−0,4×27=27,6g