Khí A có tỉ khối đối với khí oxi là 1,8125 và trong A có 82,76 % C còn lại la H
a) Hãy xác định công thức phân tử của A
b) tính thể tích không khí cần dùng để đốt cháy hoàn toàn 4,48 lít khí A. Sau phản ứng thu được bao nhiêu lít khí CO2. Biết các khí đó ở đktc

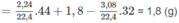
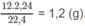
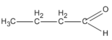 (butanal)
(butanal)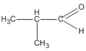 (2-metylpropanal)
(2-metylpropanal)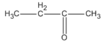 (butan-2-ol)
(butan-2-ol)
\(M_A=1,8125.32=58\left(\dfrac{g}{mol}\right)\\ \rightarrow\left\{{}\begin{matrix}m_C=58.82,76\%=48\left(g\right)\\m_H=58-48=10\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}n_C=\dfrac{48}{12}=4\left(mol\right)\\n_H=\dfrac{10}{1}=10\left(mol\right)\end{matrix}\right.\\ CTHH:C_4H_{10}\)
\(n_{C_4H_{10}}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2C4H10 + 13O2 --to--> 8CO2 + 10H2O
0,2 0,8
=> VCO2 = 0,8.22,4 = 17,92 (l)