Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{21,6}.100\%\approx25,93\%\\\%m_{Fe_2O_3}\approx100-25,93=74,07\%\end{matrix}\right.\)

Đáp án A
Đặt công thức của hai muối là RCO3
Ta có: nCO2= 10,08/22,4= 0,45 mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
Theo PT ta có: nRCO3= nRCl2= nCO2= 0,45 mol
→mRCl2- mRCO3= 0,45. (R+71)- 0,45. (R+60)= 4,95 gam
→Muối sau phản ứng tăng so với trước phản ứng là 4,95 gam

Đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]() = 6,12 gam
= 6,12 gam
→![]() gam →
gam →
![]() mol
mol
→ ![]() gam →
gam →
![]() mol.
mol.
![]()
![]() gam
gam
![]() mol
mol
![]()
![]()
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
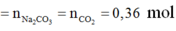
![]()
![]()
K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra
⇒ khí còn lại bị hấp thụ.
![]()
trong A chứa 2 gốc CH3COO-
⇒ gốc còn lại cũng là gốc axit đơn chức
⇒ nkhí còn lại = nA = 0,12 mol.
⇒ Mkhí còn lại =
![]()
khí còn lại là C2H4.
⇒ là (CH3COO)2(CH2=CH-COO)C3H5
⇒ a = 0,12 . 230 = 2,76
![]() mol
mol
⇒ x = 0,38 ÷ 0,19 = 2.
Muối gồm 0,12 mol
![]() ;
;
0,24 mol CH3COONa; 0,02 mol NaCl
=> b = 0,12.94 + 0,24.82 + 0,02.58,5 = 32,13
=> a + b + x = 61,73 gam

Chọn đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]()
![]()
→ n C O 2 = 0 , 09 mol ⇒ n C = 0 , 09 mol.
![]()
→ n H 2 O = 0 , 12 mol ⇒ n H = 0 , 24 mol.
![]()
![]()
⇒ n O = 0 , 09 m o l
⇒ C : H : O = 0 , 09 : 0 , 24 : 0 , 09 = 3 : 8 : 3 ⇒ Z là C3H8O3.
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
![]()
M K = 0 , 625 x 32 = 20 g/mol ⇒ K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra ⇒ khí còn lại bị hấp thụ.

Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 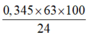
= 90,5625 gam

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam

a)
Gọi $n_{Fe} = a(mol) ; n_{Al} =b (mol) \Rightarrow 56a + 27b = 11(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
Theo PTHH : $n_{H_2} = a + 1,5b = \dfrac{8,96}{22,4} = 0,4(2)$
Từ (1)(2) suy ra : a = 0,1 ; b = 0,2
$\%m_{Fe} = \dfrac{0,1.56}{11}.100\% = 50,9\%$
$\%m_{Al} = 100\% - 50,9\% = 49,1\%$
b) $n_{HCl} = 2n_{H_2} = 0,8(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,8}{0,4} = 2M$
c)
$C_{M_{FeCl_2}} = \dfrac{0,1}{0,4} = 0,25M$
$C_{M_{AlCl_3}} =\dfrac{0,2}{0,4} = 0,5M$
\(Gọi\ n_{H_2} = n_{H_2SO_4} = a(mol)\)
Bảo toàn khối lượng :
\(30,5 + 98a = 2a + 97,7\\ \Rightarrow a = 0,7(mol)\\ \Rightarrow V = 0,7.22,4 = 15,68(lít)\)
Gọi \(n_{H_2}=n_{H_2SO_4}=a\text{ ( mol )}\)
Áp dụng định luật bảo toàn khối lượng ta có :
30,5 + 98a = 2a + 97,7
⇒ a = 0,7 ( mol )
=> V = 0,7 . 22,4 = 15,68 ( lít )