Hợp chất khí có công thức tổng quát là RO2. Biết rằng 8,8 gam hợp chất khí này có thể tích gấp hai lần thể tích của 3,2 gam khí O2 ở cùng điều kiện nhiệt độ và áp suất. Hãy xác định công thức hóa học của hợp chất khí
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


=> nRO2 = 3,36 / 22,4 = 0,15 mol
=> MRO2 = 6,6 / 0,15 = 44 (g/mol)
=> MR = 44 - 16 x 2 = 12 ( g/mol)
=> R là nguyên tố cacbon ( KHHH: C)
=> CTHH đúng của hợp chất: CO2
n=V/22,4=3,36(l)
M=m/n=44g/mol
mà o2 =32 dvc
MR =44_32=12g/mol =>ntố cacbon

Gọi công thức hợp chất hữu cơ là CxHyOz (x,y,z nguyên dương)
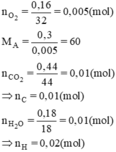
mO = mA – (mC + mH) = 0,3 - (0,01.12 + 0,02.1) = 0,16(g)
⇒ nO = 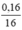 = 0,01(mol)
= 0,01(mol)
nC : nH : nO = 0,01 : 0,02 : 0,01 = 1 : 2 : 1
⇒ công thức phân tử (CH2O)n
Ta có: mA = 30n = 60 ⇒ n = 2
⇒ Công thức phân tử của A là C2H4O2

Đáp án : A
3,7g X ứng với 1 , 6 32 = 0,05 mol => MX = 74
Đốt 1g X → nCO2 > 0,7 lít
=> Số C của X = n CO 2 n X > 0 , 7 22 , 4 1 74 = 2,3125
=> X có 3 C; X là C3H6O2 (HCOOC2H5)

Chọn đáp án C
♦ giải đốt 1 , 76 g a m T + 0 , 075 m o l O 2 → t 0 7 C O 2 + 6 H 2 O
BTKL có m C O 2 + m H 2 O = 1 , 76 + 0 , 075 × 32 = 4 , 16 g a m
Giả thiết n C O 2 : n H 2 O = 7 : 6 → n C O 2 = 0 , 07 m o l ; n H 2 O = 0 , 06 m o l
bảo toàn có n O trong T = 0,05 mol
→ tỉ lệ n C : n H : n O = 7 : 12 : 5
→ CTPT của T là C 7 H 12 O 5 . Số O = 5; axit 2 chức có 4O
→ còn 1O của nhóm -OH ancol chưa phản ứng nữa mới đủ.
→ 2 ancol có cùng số C và 1 ancol đơn chức; 1 ancol còn lại hai chức.
ancol 2 chức, axit 2 chức thì phải từ C2 trở đi
→ 7 = 2 × 2 + 3
→ CTCT của T là C 2 H 5 O O C - C H 2 - C O O C H 2 C H 2 O H
→ 2 ancol là ancol etylic ( C 2 H 5 O H ) và etylen glicol ( C 2 H 4 ( O H ) 2 )

giải ra co2 0.1 mol h20 0,1 mol suy ra mol oxi rồi giải bt

bn copy câu trả lời về cho mk đi
mk sao chép đường dẫn ko được
\(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)=>n_{RO_2}=0,2\left(mol\right)\)
=> \(M_{RO_2}=\dfrac{8,8}{0,2}=44\left(g/mol\right)\)
=> MR = 12(g/mol)
=> R là C
=> CTHH: CO2