Đốt cháy hoàn toàn 4,48 lít hỗn hợp 2 anken X và Y (đktc) là đồng đẳng kế tiếp nhau thu được 11,2 lít CO2 (đktc). Tính % thể tích mỗi anken hỗn hợp ban đầu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a/
nX=4,48\22,4=0,2 mol
nCO2=11,2\22,4=0,5 mol
CTTQ của hh 2 anken là CnH2n
PTHH:CnH2n+3n\2O2→nCO2+nH2O
Ta có tỉ lệ: 1\0,2 =n\0,5
=>n=2,5 => công thức là C2H2, C3H6

Gọi CTPT của anken là C n H 2 n
CTPT trung bình của 2 amin là C m ¯ H 2 m ¯ + 3 N
PTHH:
C n H 2 n + 3 n 2 O 2 → n C O 2 + n H 2 O
a → 3 na 2 → an
C m ¯ H 2 m ¯ + 3 N + 6 m ¯ + 3 4 O 2 → m ¯ C O 2 + 2 m ¯ + 3 2 H 2 O + 1 2 N 2
b → 6 m ¯ + 3 b 4 → b ¯ m
n C O 2 = 0 , 1 = a n + b m ¯ 0 , 2025 = 3 an 2 + 6 m ¯ + 3 b 4 ⇒ b = 0 , 07 ⇒ a n + 0 , 07 m ¯ = 0 , 1 ⇒ m ¯ < 2
→ 2 amin là C H 5 N v à C 2 H 7 N
Đáp án cần chọn là: C

Chọn đáp án A
Câu này có thể suy luận nhanh như sau :
+ Với B và C là hai đồng phân (cùng CTPT) mà chỉ có phản ứng đốt cháy thì không thể phân biệt được nên ta sẽ loại hai đáp án này ngay .
+ Với A và D nếu 50/50 thì có thể chọn D vì các bài toán Hóa Học nếu chặn khoảng thường phải < hơn chứ hiếm khi > một giá trị nào đó.
Nếu chơi đẹp ta có thể giải như sau:
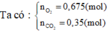
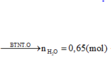
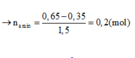

![]()
Tới đây ta có thể chọn A ngay vì nếu các amin có nhiều hơn 2 C thì số mol CO2 sẽ vô lý ngay.

Đáp án C
Hướng dẫn
Đặt CTTB của hai anken (olefin) là C n - H 2 n -
Số mol của hỗn hợp hai anken = 8 , 96 22 , 4 = 0,4 mol
C n - H 2 n - + 3 n - 2 O 2 → n - C O 2 + n - H 2 O
mol: 0 , 4 → 0 , 4 n - → 0 , 4 n -
Theo giả thiết và (1) ta có :
m C O 2 - m H 2 O = 44.0,4 n - - 18.0,4 n - = (m + 39) - m = 39 => n - = 3,75
Vì hai anken là đồng đẳng kế tiếp và có số nguyên tử cacbon trung bình là 3,75 nên suy ra công thức phân tử của hai anken là C3H6 và C4H8
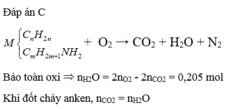
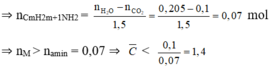


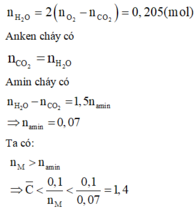

Số nguyên tử Cacbon trung bình = \(\dfrac{V_{CO_2}}{V_{hh}} = \dfrac{11,2}{4,48} = 2,5\)
Suy ra : Hai anken là \(C_2H_4(x\ lít)\ ; C_3H_6(y\ lít)\)
Bảo toàn nguyên tố với C :
\(V_{CO_2} = 2x + 3y = 11,2(1)\)
\(V_{hỗn\ hợp} = x + y = 4,48(2)\\ (1)(2) \Rightarrow x = 2,24 ; y = 2,24\\ \Rightarrow \%V_{C_2H_4}=\%V_{C_3H_6} = \dfrac{2,24}{4,48}.100\% = 50\%\)