Tính khối lượng mol phân tử các chất sau: a. Chất A có tỉ khối hơi so với không khí bằng 2,07 b. Thể tích hơi của 3,3gam chất X bằng thể tích của 1,76gam khí oxi (ở cùng điều kiện, nhiệt độ, áp suất)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Dùng công thức M = 29d = 60 đvC
b) nA = nO2 = 1,76 : 32 = 0,055 mol \(\Rightarrow\) MA = 3,3 : 0,055 = 60 đvC

a/ => MA = 2,07 x 29 = 60,03 (gam/mol)
b/ nO2 = 1,76 / 32 = 0,055 mol
Vì ở cùng điều kiện nhiệt độ, áp xuất, tỉ lệ thể tích chính là tỉ lệ về số mol
=> nX = 0,055 mol
=> MX = 3,3 / 0,055 = 60 (g/mol)
a) Dùng công thức M = 29d = 60 g/mol
b) nA = nO2 = 1,76 : 32 = 0,055 mol \(\Rightarrow\) MA = 3,3 : 0,055 = 60 g/mol

Vì dA/không khí = 2,07 ⇒ MA = 2,07.29 = 60
(vì Mkhông khí = 29)

Gọi công thức hợp chất hữu cơ là CxHyOz (x,y,z nguyên dương)
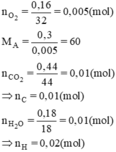
mO = mA – (mC + mH) = 0,3 - (0,01.12 + 0,02.1) = 0,16(g)
⇒ nO = 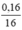 = 0,01(mol)
= 0,01(mol)
nC : nH : nO = 0,01 : 0,02 : 0,01 = 1 : 2 : 1
⇒ công thức phân tử (CH2O)n
Ta có: mA = 30n = 60 ⇒ n = 2
⇒ Công thức phân tử của A là C2H4O2

Đáp án A
Do ở cùng điều kiện nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol.
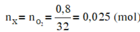
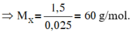
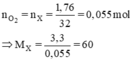

\(a,M_A=29.2,07\approx 60(g/mol)\\ b,n_X=n_{O_2}=\dfrac{1,76}{32}=0,055(mol)\\ \Rightarrow M_X=\dfrac{3,3}{0,055}=60(g/mol)\)
29 ở đâu và 32 ở đâu ạ