Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(Mg + 2HCl \to MgCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ Zn + 2HCl \to ZnCl_2 + H_2\)
b)
Gọi : \(n_{H_2} = a(mol) \Rightarrow n_{HCl} = 2a\)
Bảo toàn khối lượng :
\(13,5 + 2a.36,5 = 66,75 + 2.a\\ \Rightarrow a = 0,75\\ \Rightarrow V = 0,75.22,4 = 16,8(lít)\)
a) Mg + 2 HCl -> MgCl2 + H2
2Al + 6 HCl -> 2 AlCl3 + 3 H2
Fe + 2 HCl -> FeCl2 + H2
Zn + 2 HCl -> ZnCl2 + H2
b) mY-mX=mCl
<=> mCl= 66,75-13,5=53,25(g)
=>nCl=53,25/35,5=1,5(mol)
=> nH2= nCl/2= 1,5/2=0,75(mol)
=>V=V(H2,đktc)=0,75.22,4=16,8(l)

2Al+3H2SO4->al2(SO4)3+3H2
Fe+H2SO4->FeSO4+H2
Gọi x,y tương ứng là số mol của Al và Fe:
Ta có: 27x+56y=11 (1)
nH2=0,4 mol
1,5x+y=0,4 (2)
Giải hệ(1),(2):x=0,2;y=0,1
mAl=0,2.27=5,4g
%Al=\(\dfrac{5,4.100}{16,6}\)=32,53%
=>%Fe=67,47%
m H2SO4=0,4.98=39,2g
c) m muối=0,1.342+0,1.152=49,4g

Gọi x, y lần lượt là số mol Al, Fe
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ Tacó:\left\{{}\begin{matrix}27x+56y=0,83\\1,5x+y=0,025\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,01\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{Al}=0,27\left(g\right)\\m_{Fe}=0,56\left(g\right)\end{matrix}\right.\)

Đáp án B
Dùng phương pháp đường chéo tính được mol CO2 là 0,2 mol và H2 là 0,15 mol.
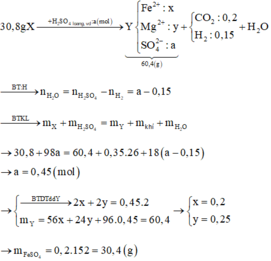

Đáp án B
Cho 46,37 gam hỗn hơp H vào dung dịch chứa H2SO4 và HNO3 (tỉ lệ mol là 37:6) thu được 0,11 mol hỗn hợp khí T và dung dịch X
Tăng giảm khối lượng:
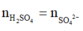
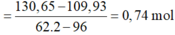
![]()
Gọi a, b, c lần lượt là số mol của H2, NO và H2O
=> a + b = 0,11
Bảo toàn nguyên tố N:
![]()
Bảo toàn H:
![]()
Bảo toàn khối lượng:
![]()
![]()
Giải hệ: a=0,01; b=0,1; c=0,75.
Gọi số mol Al, Zn, Fe3O4 và CuO trong H lần lượt là x, y, z, t
![]()
Bảo toàn điện tích:
![]()
Khối lượng chất tan trong X:
![]()
![]()
Nhiệt phân chất tan trong Y ta thu được rắn G gồm Al2O3, ZnO, Fe2O3 và CuO:
![]()
= 51,67
Giải hệ: x=0,1; y=0,15; y=0,06; t=0,25
BTKL:
![]() = 243,35
= 243,35
![]()


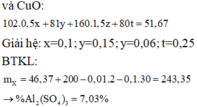
a) PTHH: \(Ca+H_2SO_4\rightarrow CaSO_4+H_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
b) Ta có: \(\Sigma n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo các PTHH, ta thấy \(n_{H_2SO_4}=n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,5\cdot98=49\left(g\right)\)
Mặt khác: \(m_{H_2}=0,5\cdot2=1\left(g\right)\)
Bảo toàn khối lượng: \(m_{hh}=m_{muối}+m_{H_2}-m_{H_2SO_4}=68+1-49=20\left(g\right)\)